商机详情 -
药学研究项目
中药抗tumor研究已从直接杀伤细胞转向表观遗传调控领域。以黄芩苷为例,其可通过抑制组蛋白去乙酰化酶(HDAC)活性,上调p21基因表达,诱导肿瘤细胞周期阻滞。实验显示,黄芩苷处理后的肝ancer细胞,其H3K27ac修饰水平明显升高,促进抑ancer基因转录。另一机制是中药多糖对DNA甲基化的调节,如茯苓多糖可降低结直肠癌细胞中DNMT3B表达,恢复MLH1等抑ancer基因的甲基化沉默。此外,中药复方(如四君子汤)可通过调节miRNA表达(如上调miR-34a),抑制tumor干细胞自我更新。这些表观遗传调控研究,为中药抗tumor提供了新的分子靶点,也解释了其“多靶点、低毒性”的优势。斑马鱼模型评价眼毒***学研究项目
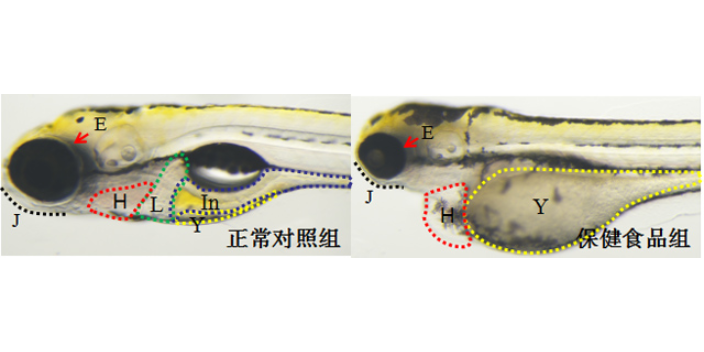
神经退行性疾病药物研究面临靶点难发现、血脑屏障穿透难、临床转化效率低等重大挑战,是药物研究领域的难点与焦点。杭州环特生物凭借斑马鱼在神经药物研究中的独特优势,构建了帕金森病、阿尔茨海默病、癫痫等多种神经疾病斑马鱼药物研究模型,为神经小分子药物研究开辟新路径。斑马鱼的中枢的神经系统发育与人类高度保守,具有血脑屏障结构,且行为学表型易观测,在药物研究中可实现对神经保护、神经修复、神经递质调节等药物效果的精细评估。在药物研究中,环特生物通过分子标记、行为学分析、电生理检测等技术,多方面解析药物研究中化合物的神经药理活性与作用机制,突破传统神经药物研究体外模型与哺乳动物模型的局限,为攻克神经退行性疾病提供高效药物研究平台。生物药安评机构药物临床前研究实验。
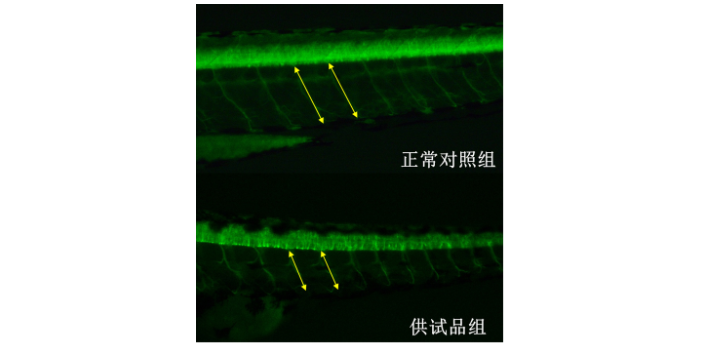
中药现代化药物研究是传承与创新中医药的关键路径,通过现代药物研究技术阐明中药有效成分、作用机制与安全性,是中药走向国际化的关键。杭州环特生物将斑马鱼技术应用于中药小分子药物研究,构建了中药现代化药物研究创新平台,为中药药物研究提供科学支撑。在中药药物研究中,环特生物利用斑马鱼模型开展中药的单体、复方、提取物的活性筛选、药效评价与毒理研究,通过药物研究技术精细识别中药中的药效物质基础,解析多成分、多靶点协同作用机制,同时评估中药的急性毒性、长期毒性与发育毒性。斑马鱼药物研究模型解决了传统中药药物研究周期长、成本高、机制不明等难题,为中药现代化药物研究提供高效、可视化、标准化的技术手段,推动中药药物研究与国际接轨。
药物研究的行业标准与规范制定是推动药物研究行业规范化、标准化发展的关键,也是药物研究技术得到宽泛认可的基础。杭州环特生物作为斑马鱼药物研究技术的全球带领者,积极参与药物研究行业标准与规范的制定工作。环特生物牵头或参与制定多项斑马鱼药物研究技术指南、行业标准与技术共识,将自身药物研究技术经验与行业共享,推动斑马鱼药物研究技术的标准化、规范化应用。在药物研究服务中,环特生物严格遵循已制定的药物研究标准与规范,确保药物研究数据的一致性、可靠性与可比性。通过参与药物研究行业标准制定,环特生物不仅提升自身在药物研究领域的有影响力性,更推动整个药物研究行业的高质量、规范化发展。利用斑马鱼模型评价帕金森病防治作用。

研究人员对32名肝cancer患者的多区域类organ进行了基因组分析,发现明显的基因组异质性。研究人员发现,包括P1、P4、P6和P23在内的一个亚组患者在多区域样本中cancer突变负荷(TMB)存在明显差异;不同区域的cancer样本在基因突变和拷贝数变化方面存在差异(图2A);一些与肝cancer相关的基因在不同区域的表达存在差异(图2F)。为了验证基因组和相关转录组的异质性是否可能导致药物敏感性的异质性,研究人员用79例患者的、255例PDOs研究了PLC前列药物索拉非尼(sorafenib)和乐伐替尼(lenvatinib)靶基因的表达,结果显示,一些患者(如P6和P32),在来自不同区域类organ中的靶基因表达存在很大差异,这表明可能存在cancer内药物反应的异质性。新一轮基本药物目录调整在即。药物功效评估
利用斑马鱼模型实验评价通便功效。药学研究项目
人工智能(AI)正深刻改变药物筛选的逻辑。深度学习模型可处理海量生物医学数据,从基因组、蛋白质结构到临床病例,挖掘传统方法难以发现的模式。例如,AlphaFold2预测的蛋白质结构数据库(AlphaFoldDB)已覆盖超2亿种蛋白,为基于结构的药物设计(SBDD)提供精细靶点模型。生成式AI(如DiffusionModel)则能直接生成具有特定药效团的分子结构,英国BenevolentAI公司利用其平台,在6个月内发现针对肌萎缩侧索硬化症(ALS)的潜在药物分子,较传统方法提速5倍。此外,强化学习算法可模拟化合物优化过程,自动调整分子骨架、官能团,生成“类药物的性”更高的候选物。AI与高通量筛选的结合,使药物发现从“大海捞针”转向“精细制导”,据统计,AI辅助筛选使先导化合物发现成功率提升3倍。药学研究项目