商机详情 -
山东重组药物支原体检测NAT法
来源:
发布时间:2025年11月13日
可比性验证是支原体检测 NAT 方法替代传统检测方法的关键依据,法规明确要求需将 NAT 法与药典规定的传统方法进行检测限(LOD)对比。若以 NAT 法替代培养法,需证实其检测限≤10CFU/mL;替代指示细胞培养法时,每种被测支原体的检测限需≤100CFU/mL。对比实验需采用相同样本同步开展 NAT 检测与传统方法检测,通过 CFU 可比性分析,确保两种方法的检测结果具有一致性。这一要求既保障了新方法的检测效能不低于传统标准,又为生物制品企业切换检测方法提供了合规依据,兼顾了效率提升与质量安全。
支原体污染来源多样,包括人源、动物源及环境,需多方位监测。山东重组药物支原体检测NAT法
AdvSHENTEK 一体化支原体检测试剂盒具备较广的检测覆盖范围与极强的专属性,能应对各类潜在污染风险。试剂盒可准确检出近 200 种微生物,包括支原体、螺原体、无胆甾原体、虫原体及中间原体,覆盖生物药生产中常见的污染菌株类型。经严格验证,对鸡滑支原体、精氨酸支原体、猪鼻支原体、肺炎支原体等多种菌株,在 10CFU/mL 和 100CFU/mL 浓度下的阳性检出率均达到 24/24,其中包含多个 ATCC 标准菌株。同时,试剂盒专属性强,无交叉干扰现象,能有效区分目标菌株与其他非目标微生物,避免假阳性结果,确保检测数据的准确性,为企业排查支原体污染提供可靠保障。
吉林干细胞产品支原体检测技术服务湖州申科支原体验证菌株溯源至 ATCC/CVCC,标定 10CFU/100CFU,满足验证需求。
MycoSHENTEK® 支原体 qPCR 检测试剂盒(2G)完全符合 EP 2.6.7 的全部验证要求,其检测灵敏度、特异性、耐用性均按药典标准完成完整性能验证,具备替代培养法和指示细胞培养法的合规资质。该试剂盒针对新型生物制品的检测痛点优化升级,经多种支原体菌株验证,灵敏度稳定达到 10 CFU/mL,满足法规对替代培养法的要求。同时,产品遵循 ISO13485 体系认证和 GMP-like 生产标准,可提供完整的验证报告、质检报告及菌株溯源文件,全程贴合各国药典监管要求,为企业合规检测提供坚实支撑。
全球主流药典均认可 NAT 法作为支原体检测的替代方法,但明确要求需经过充分验证并证明与传统方法的可比性。欧洲药典(EP)2.6.7 规定 NAT 法可作为替代方法,需开展供试品抑制性验证;美国药典(USP)63&77 要求替代方法需与培养法、指示细胞培养法均具备可比性,且 USP<77> 专门针对支原体 NAT 法的验证与检测制定了规范;日本药典(JP)G3-14-170 允许经适当验证后的 NAT 法替代传统方法;中国药典 3301 及相关指导原则明确,CAR-T、干细胞等新型产品可采用 NAT 法,但需充分验证其最低检出限不低于药典方法,早期需与药典方法并行使用。此外,各国法规均强调,NAT 法的选择、开发与应用需基于科学依据,充分考虑培养基、生产工艺、潜在污染菌株等因素。
支原体检测过程中,需严格遵循 “先阴后阳” 操作原则,避免交叉污染。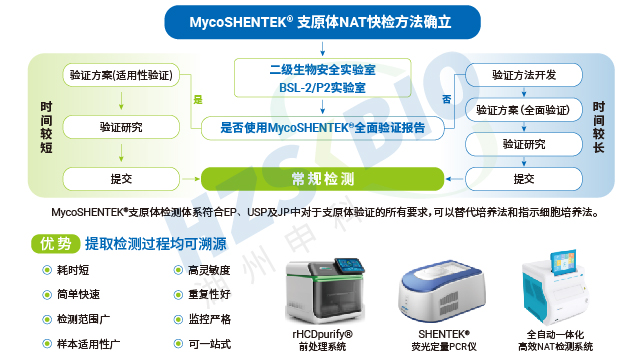
对照菌株的合理配置是支原体培养法检测准确性的重要保障,湖州申科严格遵循 USP 标准制定菌株使用规范。每次检测需至少包含两株已知支原体菌株:一株为葡萄糖发酵型(如肺炎支原体或其等效种株),另一株为精氨酸水解型(如口腔支原体),通过两类菌株的平行对照,覆盖常见支原体检测场景。特殊场景下需额外补充菌株:检测昆虫细胞系时,需纳入螺原体(如 S.citri ATCC 29747、S.melliferum ATCC 29416 或等效菌种菌株),这类菌株营养需求更苛刻,且需匹配昆虫细胞系对应的较低孵化温度,确保特殊样品检测的针对性与有效性,避免因菌株配置不全导致漏检风险。
一体化支原体检测卡盒集成全流程,相当于迷你 qPCR 实验室,普通环境即可使用。重庆生物制品支原体检测培养法生物制品终末灭菌难度大,需通过全流程支原体检测控制污染风险。山东重组药物支原体检测NAT法
取样量的科学设计直接影响支原体检测的代表性与灵敏度,需结合样品总体积、基质特性综合考量。法规建议:产品总体积大于1000mL的按无菌检查法取样,10-1000mL 取总体积的 1%,1-10mL 取 100μL,小于1mL的需采用替代取样方案。实际检测中,取样体积越大,灵敏度越高,但需平衡洗脱液消耗与重复检测需求。此外,支原体兼具胞内胞外生存特性,只检测上清会导致漏检,需采用细胞裂解等处理方式,确保覆盖全部污染靶点,提升检测结果的真实性。
山东重组药物支原体检测NAT法
上一篇:
江西细胞疗法产品支原体检测方法学验证
下一篇:
浙江疫苗产品支原体检测验证菌株