商机详情 -
可吸收缝合线医疗器械体内药效学评价空白线
医疗器械体内药效学评价在针对AMP类植入器械时,需重点关注其独特的免疫调节功能,这是区别于传统Antibiotic的主要特征。在构建的植入器械模型中,除通过平板计数等常规方法检测局部细菌载量以评估直接抑菌效果外,更需深入解析其对宿主免疫应答的调控作用。具体而言,采用流式细胞术对创面部位组织的免疫细胞亚群进行精细分析,重点监测M1型与M2型巨噬细胞的比例变化,以此判断AMP是否能平衡炎症反应、避免过度免疫损伤;同时通过多重免疫检测技术测定细胞因子表达谱,包括IL-10、TGF-β等关键分子的水平波动。这种兼顾抑菌效能与免疫调节的评价体系,不仅能反映AMP的综合生物活性,更能揭示其通过调节宿主免疫功能增强anti-infective能力的独特机制,为该类新型抑菌材料的临床转化提供更科学的依据。动物实验中缝合线的抗张力强度变化,是其医疗器械体内药效学评价的指标;可吸收缝合线医疗器械体内药效学评价空白线
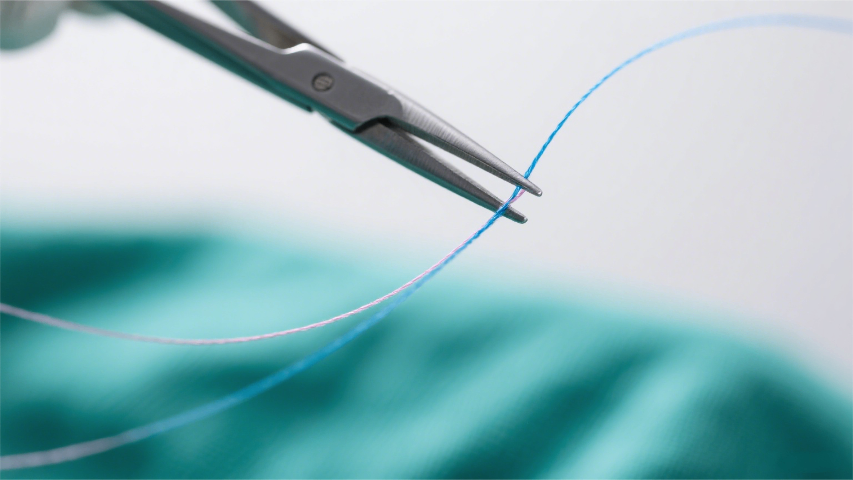
针对三氯生 - 银离子复合缝合线的协同抑菌效果,可构建小鼠模型场景。在背部制造皮肤创面并接种 MRSA,分别采用复合缝合线、单纯三氯生缝合线、单纯银离子缝合线及普通缝合线进行缝合。抑菌协同性评价采用棋盘法计算部分抑菌浓度指数(FICI),结合创面组织的细菌载量动态变化,明确复合配方是否优于单一成分。同时,检测缝合线周围组织的三氯生与银离子浓度,分析两者释放速率的匹配性。组织修复评价通过检测创面愈合率等参数,判断复合成分对创面修复的影响。广州手术膜医疗器械体内药效学评价品牌医疗器械体内药效学评价结合qPCR检测碘离子器械的耐药基因表达;
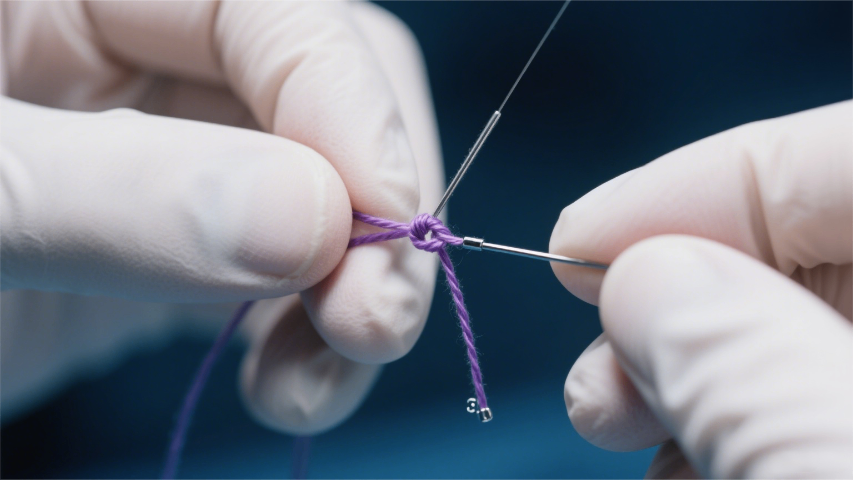
抑菌缝合线的体内药效学评价需依托标准化模型开展系统验证。实验中,先将金黄色葡萄球菌标准化菌液接种于大鼠背部切口,构建模型,随后分别植入含抑菌涂层的缝合线与普通缝合线作为对照。术后定期采集伤口组织样本,通过平板计数法精确测定细菌载量变化,同时记录伤口情况、消退时间及分泌物性质,动态评估局部控制效果。此外,需密切监测动物脓毒症发生率及死亡率,以反映抑菌缝合线的预防作用。还需通过组织病理学检查观察肉芽组织形成、胶原沉积及炎症细胞浸润情况,验证抑菌成分对正常组织修复过程无抑制作用。通过多维度指标的综合比较,可为抑菌缝合线的临床应用提供实验依据。
抑菌缝合线的体内药效学评价,需遵循标准化实验流程开展系统验证。实验初期,将金黄色葡萄球菌标准化菌液接种至大鼠背部切口,构建模拟临床术后的病理模型,再将含抑菌涂层缝合线与普通缝合线分组植入,通过对照设计区分抑菌效果差异。术后监测需聚焦关键指标:按固定周期采集伤口组织,用平板计数法精确测定细菌载量变化,同时详细记录伤口情况、渗液量及性质、炎症持续时间,以此评估缝合线对局部的控制能力;同步追踪动物脓毒症发生率与死亡率,验证对严重并发症的预防作用。此外,组织病理学检查需观察肉芽组织生长密度、胶原纤维排列及炎症细胞浸润程度,确保抑菌成分不影响组织修复。通过对多维度数据的综合解析,可为抑菌缝合线的临床应用提供科学且可靠的实验支撑。医疗器械缝合线的体内药效学评价,能否只依靠动物实验来反映其在人体中的作用?
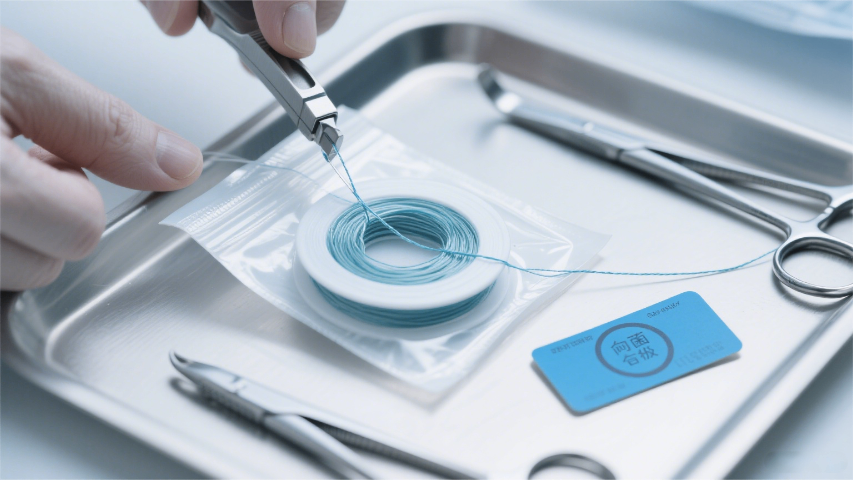
随着纳米技术在医疗器械领域的渗透,纳米材料独特的生物效应与潜在毒性已成为生物学评价的主要焦点。纳米医疗器械生物学评价分技委年会多次强调,需针对纳米材料的特殊性制定差异化评价标准,目前已推动多项专项规范的制定与完善,填补了传统评价体系的空白。在医疗器械体内药效学评价中,必须系统考量纳米材料的固有特性:尺寸效应可能使其穿透生物屏障,引发特殊的细胞应答;表面电荷会影响与生物分子的相互作用,改变其在体内的分布与代谢;离子释放特性则直接关联长效毒性与功能持续性。这些因素的综合作用,可能偏离常规材料的安全性与有效性表现,甚至引发免疫原性异常或组织损伤。因此,建立兼顾纳米材料特殊性的评价体系,既是保障临床应用安全的前提,也是推动纳米医疗器械创新转化的关键。医疗器械体内药效学评价通过慢性创面模型测试三氯生纳米纤维膜;四川不可吸收缝合线医疗器械体内药效学评价
医疗器械体内药效学评价通过组织载菌量检测优化三氯生浓度梯度;可吸收缝合线医疗器械体内药效学评价空白线
针对三氯生缝合线的抑菌时效性,可构建小鼠背部全层皮肤切口模型进行系统评估。实验中,将 小鼠背部脱毛后制造 1cm 标准化切口,接种 一定浓度 的金黄色葡萄球菌,随即用三氯生涂层缝合线实验组与对照组进行皮下连续缝合,每组至少 10 只小鼠。术后每日观察切口肿胀、渗液情况并评分,于术后不同天数处死小鼠,采集缝合线及周围 0.5cm 范围组织。通过超声震荡法分离缝合线表面细菌,平板计数测定活菌数;组织匀浆后进行梯度稀释培养,计算细菌载量。通过观察细菌载量降低 ,可判断三氯生缝合线在小鼠模型中的抑菌作用。可吸收缝合线医疗器械体内药效学评价空白线