商机详情 -
高脂喂养小鼠技术推广
大鼠的抓取固定大鼠的抓取斯基本同小鼠,只不过大鼠比小鼠牙尖性猛,不易用袭击方式抓取,否则会被咬伤手指,抓取时为避免咬伤,可带上帆布手套。如果进行腹腔、肌肉皮下等注射和灌胃时,同样可采用左手固定法,只是用拇指和食指捏住鼠耳,余下三指紧捏鼠背皮肤,置于左掌心中,这样右手即可进行各种实验操作。也可伸开左手之虎口,敏捷地从后,一把抓住。若做手术或解剖等,则需事先麻醉或处死,然后用细棉线绳活缚腿,背卧位绑在大鼠固定板上;尾静脉注射时的固定同小鼠(只需将固定架改为大鼠固定盒即可)。注意事项:为了减少或避免大鼠在实验中发生的应激反应,以减少对实验者的攻击损伤,这里介绍几种抓取大鼠的技巧改进:(1)在抓取前可用一条清洁的毛巾蒙住大鼠全身,大鼠处于黑暗状态下神经会有所放松,看不到实验者的动作也会降低对实验者的攻击机会;(2)一般抓取大鼠都会抓住尾巴,但是有时大鼠尾巴不在身后而在其面前,这时实验者可能在抓取鼠尾的时候被大鼠攻击。这种情况一般可以轻推其腰臀部,使之变换姿势,待鼠尾调整到身后再进行抓取;(3)由于大鼠尾部被抓起时,会应激性地排便、排尿,所以比较好在粗糙表面上垫上报纸等,做好防范措施,减轻工作量。常州卡文斯实验鼠运输全程温控,保障动物健康状态。高脂喂养小鼠技术推广
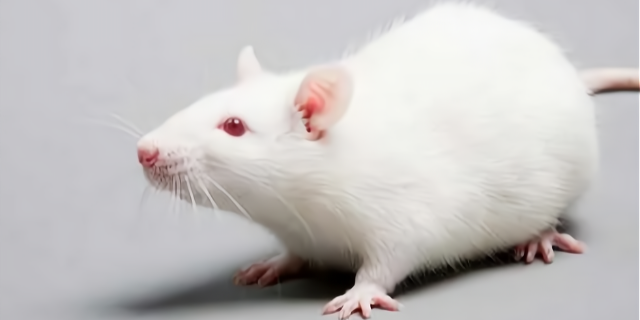
WISTAR大鼠主要用途:多用于肿块瘤体、免疫、药理、内分泌。简介:1907年由美国维斯塔尔(Wistar)研究所育成,现己遍及世界各国的实验室。我国从日本及前苏联引进,是引进较早、使用较广阔、数量较多的大鼠品系之一。特点:远交系大鼠,头部较宽、耳朵较长、尾的长度小于身长。性周期稳定,繁殖力强,产仔多,平均每胎产仔在10只左右,生长发育快。10周龄时雄鼠体重可达280~300g,雌鼠达170-260g。性情温顺。对传染病的抵抗力较强。自发性肿块瘤体发生率低。目前各地饲养的Wistar大鼠的遗传状况差异较大。NOD-Scid小鼠品系ICR/JCL小鼠是进行免疫药物筛选,复制病理模型较常用的实验动物。

实验动物是研究疾病发生/防治机制、新型药物的基础,包括实验兔子、实验猴子、实验猪、实验青蛙、实验鼠等。其中,实验鼠是继人类之后第二种完成全基因组测序的哺乳动物,其基因组中拥有人类99%蛋白编码基因的同源基因,是目前应用较广阔的实验动物,具有繁殖数量多、发育快、性成熟早、妊娠期短、饲养成本低、实验重复性高、对外来刺激敏感、遗传信息清晰等优点。实验鼠在医学领域应用十分广阔,可用于微生物学领域,研究吸血虫、锥虫、支原体、沙门氏菌等微生物寄生虫致病原理;可用于免疫学领域,研究免疫缺陷机理和相关药物;可用放射学领域,研究放射线照射剂量和辐射效应;可用于药物筛选领域,筛选药物对疾病的作用,获得每种药物治疗效果;可用于安全测试领域,判断新产品安全性;可用于遗传学领域,研究遗传病基因结构和功能,构建人类遗传病动物模型;可用于老年学领域,探究抗老老药物效果。
小鼠的抓取固定1.小鼠的抓取(1)右手提起小鼠尾巴,将其放在鼠笼盖或其他粗糙表面上(2)小鼠向前挣扎爬行时,再用左手拇指和食指抓住鼠耳和颈部皮肤抓取固定时需注意:过分用力,会使动物窒息或颈椎脱臼;用力过小,动物头部能反转来咬伤实验者的手。因此实验者必须反复练习,熟练掌握。2.小鼠的固定(1)徒手固定用右手抓取鼠尾提起,置于鼠笼或实验台向后拉,在其向前爬行时,用左手拇指和食指抓住小鼠的两耳和颈部皮肤,将鼠体置于左手心中,把后肢拉直,以无名指按住鼠尾,小指按住后腿即可。固定板固定鼠麻醉后置小鼠固定板上,取仰卧位,用胶布缠粘四肢,再用针透过胶布扎在板上,从而将小鼠固定在小鼠固定板上。(3)固定架固定让小鼠直接钻入固定架里,封好固定架的封口,露出尾巴。此装置特别适用于小鼠尾静脉注射等。实验小鼠在高海拔模拟环境中,红细胞数量和血红蛋白浓度逐渐升高以适应低氧。
卡文斯有专业的小鼠代理繁育团队,丰富的项目经验拥有10年以上SPF级动物饲养与管理经验,为国内外闻名院校、医院等提供服务,客户遍布全国各地区专业的技术团队,保障动物质量专业的项目管理体系,实时跟进小鼠繁育进程,定期项目数据反馈业务优势:严格的饲养条件温度20-26°C相对湿度40-70%噪音≤60dB氨浓度15次/小时昼夜明暗交替12h/12h严格的饲养管理要求饮用水高压灭菌后的酸化水的酸化水,PH值在、垫料及饮水的更换频率至少每周一次,所有的脏笼具,水瓶浸泡井通过高压水枪清洗后,均经高压灭菌后方可进入屏障设施,其他不能进行高压灭菌的物品则通过严格的消毒流程进入。动物的日常检查生长情况的日常观察及异常情况反馈多面的质量监测检测内容检测手段检测周期小鼠(哨兵鼠)病原委外/自检每季度1次/每月1次小鼠饲料无菌检测委外/自检每批次小鼠饮水无菌检测委外/自检每季度1次/每月1次小鼠垫料无菌检测委外/自检每季度1次/每月1次消毒效果验证。常州卡文斯实验鼠广泛应用于药物研发、基因编辑等领域。db/db实验小鼠
卡文斯实验鼠的遗传背景清晰,实验数据更具可比性。高脂喂养小鼠技术推广
在动物实验中,为了观察药物对机能功能、代谢及形态引起的变化,常需将药物注入动物体内。给药的途径和方法是多种多样的,可根据实验目的、实验动物种类和药物剂型等情况确定。实验动物常见的给用用药物使用方法法法式有:口服、静脉注射、腹腔注射、皮下注射、肌肉注射、椎管内注射、脑室内注射、皮内注射、淋巴腔注射、鼻腔和舌下给药等多种。灌胃法小鼠灌胃方法比较简单,需要关注的只有两点:一是要保持小鼠的头部和颈部成一直线,方便灌胃针头进入,二是动作要轻柔,从口角进入,防止损失食道。操作步骤:1.抓住小鼠,使其头、颈和身体呈一直线。2.用1ml的注射器配灌胃针头。灌胃针头从小鼠的嘴角进入,压住舌头,抵住上颚,轻轻向内推进,进入食管后会有一个刺空感,进入食道后就可以推注药液。3.灌胃容积一般是0.1~0.2ml/10g,比较大0.35ml/10g,每只小鼠的灌胃最大容积不超过0.8ml。高脂喂养小鼠技术推广