商机详情 -
香港哺乳动物纺锤体胚胎发育
在生殖医学领域,卵母细胞冷冻保存技术作为辅助生殖技术的重要组成部分,近年来取得了进展。尤其是针对成熟卵母细胞纺锤体的冷冻保存研究,不仅关乎女性生育能力的保存,还涉及到遗传学的稳定性和安全性。成熟卵母细胞,即处于第二次减数分裂中期(MII期)的卵母细胞,其内部包含一个高度复杂且精细的纺锤体结构。纺锤体由微管组成,这些微管通过动态变化,将染色体紧密地联系在一起,并确保在细胞分裂过程中染色体的正确分离。成熟卵母细胞的纺锤体对温度变化和机械刺激极为敏感,这使得其冷冻保存过程充满了挑战。纺锤体的结构和功能在不同类型的细胞中可能存在差异。香港哺乳动物纺锤体胚胎发育
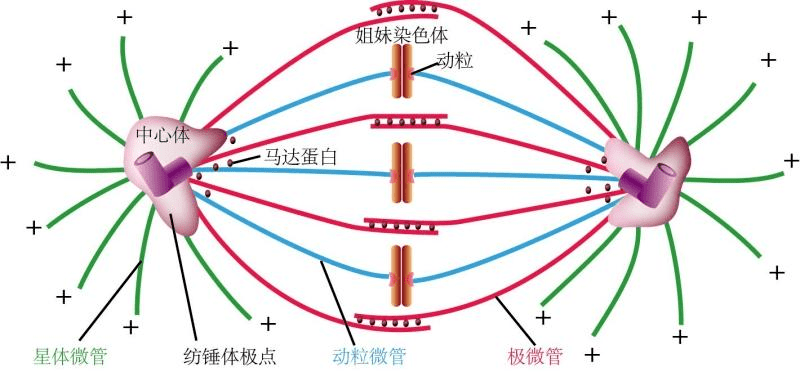
纺锤体是如何形成的(2)动粒微管连接染色体动粒与位于两极的中心体。在有丝分裂前期,一旦核被膜解聚,由相反两个方向的中心体伸出的动粒微管就会随机地与染色体上的动粒结合而俘获染色体,微管**终附着在动粒上,动粒微管把染色体和纺锤体连接在一起。在细胞分裂期的后期,分开后的染色单体被拉向两极。染色体移动由两个相互独立且同步进行的过程所介导,分别为过程A和过程B。在过程A中,在连接微管和动粒的马达蛋白的作用下,动粒微管解聚缩短,在动粒处产生的拉力使染色体移向两极。极间微管是从一个中心体伸出的某些微管与从另一个中心体伸出的微管相互作用,阻止了它们的解聚,从而使微管结构相对稳定,两套微管的这种结合形成了有丝分裂纺锤体的基本框架,具有典型的两极形态,产生这些微管的两个中心体称为纺锤极,这些相互作用的微管被称为极间微管。在有丝分裂后期过程B中,极间微管的伸长和相互间的滑行使纺锤极向两极方向移动。星体微管从中心体向周围呈辐射状分布,在有丝分裂后期过程B中,每一纺锤极上向外伸展的星体微管发出向外的力,拉动两个纺锤极向两极方向移动。美国偏光成像纺锤体提高冷冻保存效率纺锤体微管网络的动态变化揭示了细胞分裂过程中分子层面的奥秘。
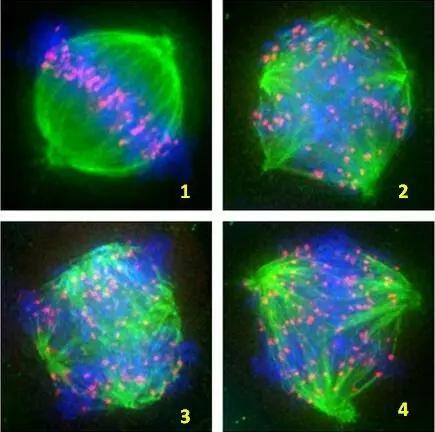
尽管纺锤体在有丝分裂与减数分裂中的作用有所不同,但两者也存在一些共性。首先,纺锤体的形成都依赖于中心体的复制和分离,以及微管的动态生长和缩短。其次,在有丝分裂和减数分裂的中期,染色体都排列在赤道板上,形成了清晰的纺锤体结构。此外,在有丝分裂和减数分裂的后期,染色体的着丝点都一分为二,导致姐妹染色单体或同源染色体分离,分别移向细胞的两极。这一过程确保了每个子细胞都能获得完整的染色体组。尽管纺锤体在有丝分裂与减数分裂中存在共性,但两者也存在明显的差异。
冷冻电镜技术(Cryo-EM)近年来在结构生物学领域取得了重大突破,也为纺锤体卵冷冻研究提供了新的视角。通过将生物样品冷冻至极低温并在电子显微镜下进行观察和成像,冷冻电镜能够揭示生物大分子的高分辨率结构,包括纺锤体微管等精细结构。这一技术不仅克服了传统电镜技术对样品制备的严格要求,还能够在接近生理状态下观察纺锤体的形态和功能,为无损观察纺锤体提供了强有力的技术支持。无损观察纺锤体技术能够实时监测冷冻过程中纺锤体的形态变化,从而准确评估冷冻保存的效果。通过对比冷冻前后纺锤体的形态和稳定性,研究者可以优化冷冻保护剂的配方和浓度,以及改进冷冻程序,减少冷冻损伤,提高解冻后卵母细胞的存活率和发育潜能。纺锤体的形成需要多种蛋白质的参与,包括微管相关蛋白和中心体蛋白等。
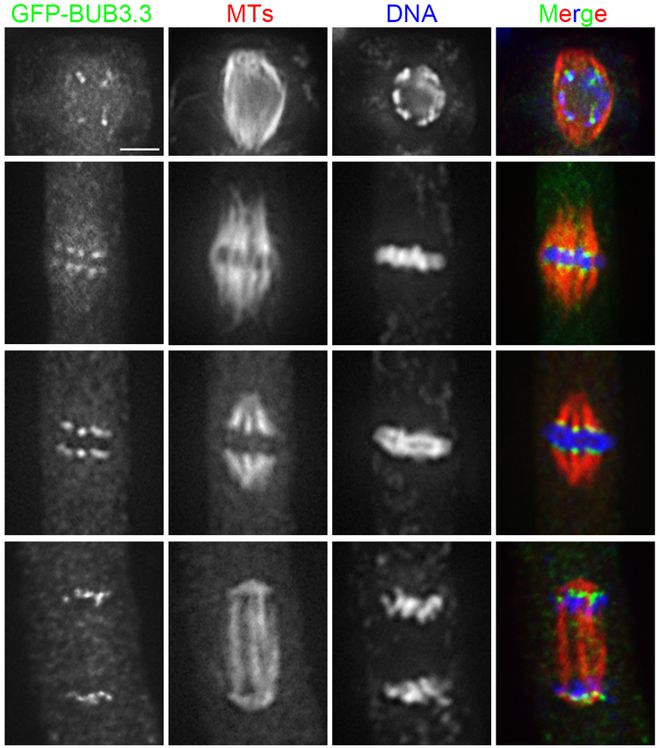
为了减少冷冻过程中纺锤体的损伤,研究者们尝试在冷冻液及解冻液中添加细胞骨架保护剂,如紫杉醇(Taxol)。紫杉醇能够稳定微管结构,防止其在低温下解聚。通过偏光成像技术,研究者可以实时监测紫杉醇对纺锤体的保护效果,评估其在冷冻保存过程中的作用机制。此外,还可以进一步观察解冻后卵母细胞的发育潜能,为临床应用提供可靠依据。无需对细胞进行固定和染色,保持细胞的活性与完整性。能够实时监测纺锤体的形态变化,评估冷冻效果。能够捕捉到细微的纺锤体形态变化,提高评估的准确性。纺锤体的功能异常与某些药物的副作用有关,如化疗药物可能干扰纺锤体的形成和功能。香港哺乳动物纺锤体胚胎发育
纺锤体在细胞分裂末期逐渐解体,为细胞质分裂做准备。香港哺乳动物纺锤体胚胎发育
核移植,又称体细胞核移植,是一种将体细胞的细胞核移入去核卵母细胞中的技术。这一技术的关键在于确保移植后的细胞核能够在卵母细胞内重新编程,恢复全能性,并引导后续的胚胎发育。自1996年克隆羊“多莉”诞生以来,核移植技术便引起了全球范围内的关注与研究热潮。纺锤体是卵母细胞在减数分裂过程中形成的关键结构,负责精确分离染色体,确保遗传信息的正确传递。然而,纺锤体对外部环境极为敏感,容易受到冷冻过程中温度波动、渗透压变化及冷冻保护剂毒性等因素的影响而发生损伤。因此,纺锤体卵冷冻技术的成功与否,直接关系到核移植后胚胎的发育潜力和质量。香港哺乳动物纺锤体胚胎发育