商机详情 -
ICSI纺锤体液晶偏光补偿器
无需染色纺锤体观察技术已逐步应用于临床辅助生殖技术中。通过该技术,医生可以在不破坏卵母细胞活性的情况下,评估其质量并选择合适的卵母细胞进行受精和胚胎移植,从而提高妊娠率和胚胎质量。无需对卵母细胞进行固定和染色处理,保留了细胞的活性与完整性。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。Polscope偏振光显微成像系统的操作和维护需要较高的专业知识和技能。纺锤体的形态变化复杂多样,需要丰富的经验和专业知识进行数据解读和结果分析。纺锤体的微管通过动态不稳定性来不断增长和缩短,从而牵引染色体运动。ICSI纺锤体液晶偏光补偿器
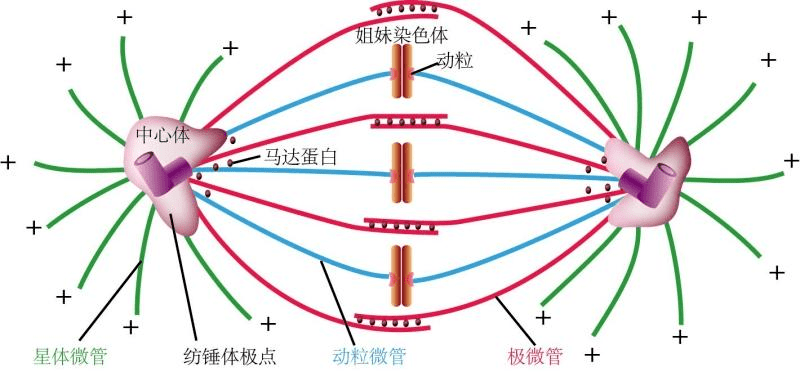
纺锤体功能分解在细胞分裂中,其主要作用有两个部分。其一为排列与分裂染色体。纺锤体的完整性决定了染色体分裂的正确性。纺锤体的正常生成是染色体排列的必要条件。纺锤体生成完毕后一般会有5-20分钟的延迟,以供细胞调整着丝点上微管束的极性,以及决定是否所有的着丝点都附着正确。此后细胞进入分裂后期,染色体分裂为两组数目相等的姐妹染色单体。同样,纺锤体的完整性决定这个分裂过程在时间和空间上的准确性。纺锤体另一功能为决定胞质分裂的分裂面。染色体分裂的同时,纺锤体中的一部分微管不随染色体分裂到两极,而停弛在纺锤体**,形成纺锤**体(centralspindle)。在纺锤中体的**为两组极性相反的微管交叠的区域,称为纺锤**区(spindlemidzone).此**区就是接下来的胞质分裂面。胞质分裂开始于分裂后期的较晚期。胞质分裂一般结束于分裂末期后1-2小时,此期间两个子细胞由中心颗粒体(midbody)连接。一般认为纺锤体的分解发生在细胞分裂末期。武汉纺锤体胚胎植入纺锤体在细胞分裂末期逐渐解体,为细胞质分裂做准备。
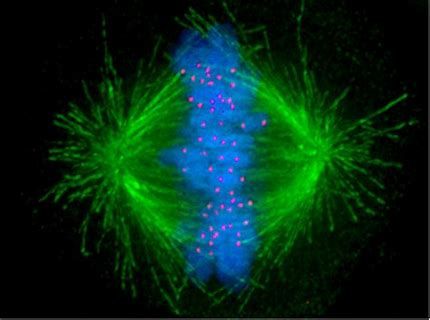
哺乳动物卵母细胞的纺锤体由微管组成,这些微管结构精细且高度动态,对温度、渗透压和机械力等外界因素极为敏感。在冷冻过程中,纺锤体容易因冰晶形成、渗透压变化或机械损伤而遭到破坏,导致染色体分离异常,进而影响卵母细胞的发育潜力和受精后的胚胎质量。选择合适的冷冻保护剂是减少纺锤体损伤的关键。然而,不同浓度的冷冻保护剂对纺锤体的影响各异,且不同哺乳动物种类之间也存在差异。因此,需要通过大量实验来优化冷冻保护剂的配方,以大限度地保护纺锤体的完整性。
为了减少冷冻过程中纺锤体的损伤,研究者们尝试在冷冻液及解冻液中添加细胞骨架保护剂,如紫杉醇(Taxol)。紫杉醇能够稳定微管结构,防止其在低温下解聚。通过偏光成像技术,研究者可以实时监测紫杉醇对纺锤体的保护效果,评估其在冷冻保存过程中的作用机制。此外,还可以进一步观察解冻后卵母细胞的发育潜能,为临床应用提供可靠依据。无需对细胞进行固定和染色,保持细胞的活性与完整性。能够实时监测纺锤体的形态变化,评估冷冻效果。能够捕捉到细微的纺锤体形态变化,提高评估的准确性。纺锤体在细胞分裂后期通过收缩力推动染色体分离。
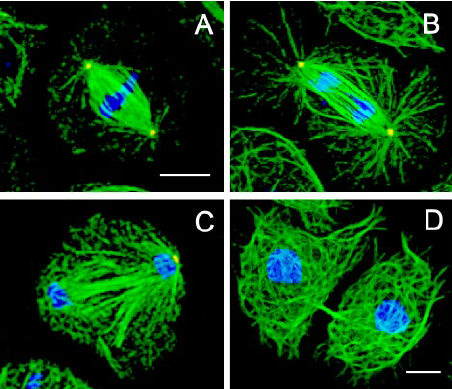
近年来,随着玻璃化冷冻技术的不断发展,成熟卵母细胞纺锤体的冷冻保存研究取得了进展。研究表明,采用玻璃化冷冻法冷冻保存的成熟卵母细胞,在解冻后其纺锤体和染色体的形态及功能均能得到较好的保持。这主要得益于玻璃化冷冻过程中避免了冰晶形成对细胞的损伤,以及冷冻保护剂对细胞的有效保护。然而,值得注意的是,尽管玻璃化冷冻法在提高解冻存活率和妊娠成功率方面取得了成效,但仍存在一些问题。例如,冷冻过程中纺锤体的微管结构可能受到低温的影响而发生解聚,导致染色体分离异常。此外,冷冻保护剂的毒性也可能对卵母细胞造成一定的损伤。为了克服这些问题,研究者们进行了大量的实验和优化工作。例如,通过改进冷冻保护剂的配方和浓度,降低其对细胞的毒性;通过优化冷冻速率和程序,减少冷冻过程中对细胞的机械损伤;以及通过筛选和评估不同冷冻载体和保存时间对卵母细胞冷冻效果的影响,寻找好的冷冻保存条件。显微镜下的纺锤体,如同精密的分子机器,引导染色体分离。美国辅助生殖纺锤体Oosight Meta
纺锤体的主要功能是在细胞分裂时牵引染色体分离,确保遗传信息的正确传递。ICSI纺锤体液晶偏光补偿器
冷冻与解冻过程中涉及多个环节,包括温度控制、时间控制、冷冻保护剂的添加与去除等。这些环节中的任何一步操作不当都可能导致纺锤体损伤。因此,需要不断优化冷冻与解冻技术,以减少对纺锤体的不良影响。近年来,研究者们通过不断尝试和优化冷冻保护剂的配方,取得了进展。例如,甘油、二甲基亚砜(DMSO)等渗透性保护剂被用于哺乳动物卵母细胞的冷冻保存中,它们能够迅速降低细胞内水分含量,减少冰晶形成。同时,一些非渗透性保护剂如蔗糖、海藻糖等也被发现对纺锤体具有一定的保护作用。ICSI纺锤体液晶偏光补偿器