商机详情 -
北京核移植纺锤体胚胎发育
卵母细胞冷冻保存主要采用两种方法:慢速冷冻法和玻璃化冷冻法。相较于传统的慢速冷冻法,玻璃化冷冻法因其更高的解冻存活率和妊娠成功率而逐渐成为主流技术。玻璃化冷冻法的基本原理是将含有生物样本的溶液在极短的时间内(如几分钟内)冷却至液氮温度,使溶液在凝固点以下形成无冰晶的半固体或固体状态。这种方法避免了冰晶形成对细胞结构的破坏,从而减少了冷冻损伤。在卵母细胞冷冻保存中,玻璃化冷冻法通过优化冷冻保护剂的浓度和冷冻速率,使卵母细胞在冷冻过程中保持其结构的完整性。纺锤体在细胞分裂过程中展现出惊人的自我组装能力。北京核移植纺锤体胚胎发育
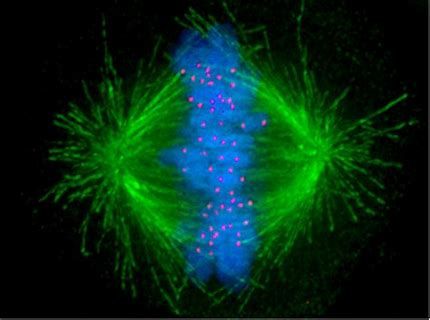
在生殖医学领域,卵母细胞的冷冻保存技术一直是研究的热点之一。尤其是针对卵母细胞内部高度复杂且精细的纺锤体结构,其冷冻过程中的稳定性与完整性直接关系到解冻后卵母细胞的存活率及发育潜能。纺锤体作为卵母细胞内部的关键结构,由微管等高分子物质有序排列而成,具有双折射性。这种特性使得纺锤体在偏振光下能够呈现出独特的形态和特征,从而被Polscope等偏振光显微镜捕捉并观察。双折射性纺锤体的形态、稳定性和完整性对于卵母细胞的正常减数分裂及胚胎发育至关重要。香港克隆纺锤体加热台纺锤体在细胞分裂中的精确调控是生物体维持遗传稳定性的关键。
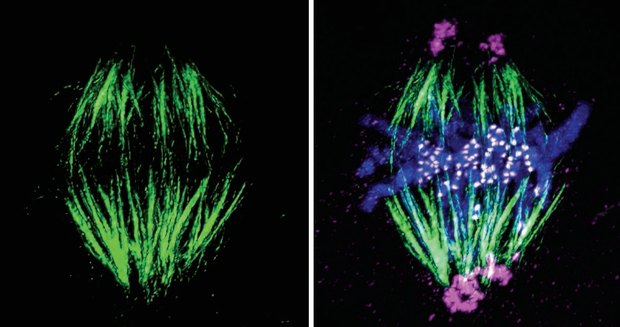
在生殖医学领域,卵母细胞的冷冻保存技术一直是研究的热点,旨在提高女性生育能力的保存与利用。然而,传统的纺锤体观察方法往往需要对卵母细胞进行固定和染色处理,这不仅破坏了细胞的活性,还限制了对其发育潜能的深入评估。偏光成像技术,特别是Polscope偏振光显微成像系统,通过利用纺锤体微管结构的双折射性,实现了对纺锤体的无损观察。这种技术无需对卵母细胞进行固定和染色,能够在保持细胞活性的同时,实时、动态地观察纺锤体的形态和变化。这不仅提高了观察的准确性和可靠性,还避免了传统染色方法可能带来的细胞损伤和误差。
无需染色纺锤体观察技术已逐步应用于临床辅助生殖技术中。通过该技术,医生可以在不破坏卵母细胞活性的情况下,评估其质量并选择合适的卵母细胞进行受精和胚胎移植,从而提高妊娠率和胚胎质量。无需对卵母细胞进行固定和染色处理,保留了细胞的活性与完整性。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。Polscope偏振光显微成像系统的操作和维护需要较高的专业知识和技能。纺锤体的形态变化复杂多样,需要丰富的经验和专业知识进行数据解读和结果分析。纺锤体微管的排列方向决定了染色体分离的方向。
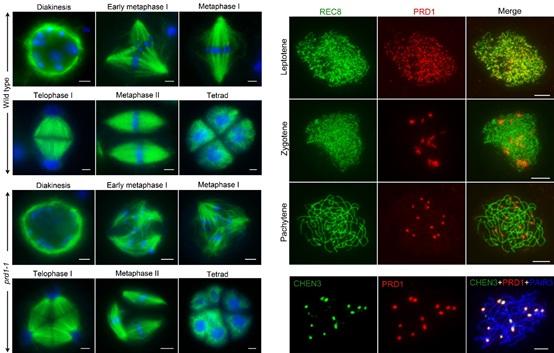
在修复纺锤体异常方面,基因转移方法可以通过将正常纺锤体相关基因导入到患者细胞中,从而恢复纺锤体的正常结构和功能。这种方法特别适用于那些由于基因缺失或突变导致纺锤体异常的患者。基因调控是通过调节基因表达水平来诊疗疾病的方法。在修复纺锤体异常方面,基因调控策略可以通过调节纺锤体相关基因的表达水平,从而恢复纺锤体的正常功能。例如,针对某些疾病中纺锤体异常导致的染色体不稳定性,基因调控策略可以通过抑制相关基因的表达,从而降低染色体的不稳定性,进而抑制细胞的生长和侵袭。 纺锤体的研究对于开发新的抗病毒药物具有重要意义。昆明卵母细胞纺锤体揭示卵母细胞关键结构
纺锤体的形成和功能受到多种信号分子的调控,如生长因子等。北京核移植纺锤体胚胎发育
纺锤体是卵母细胞在减数分裂过程中形成的一种微管结构,负责精确分离染色体。然而,纺锤体对环境温度、渗透压等外部条件极为敏感,在冷冻保存过程中容易发生损伤,导致染色体分离异常,进而影响卵母细胞的发育潜力和受精后的胚胎质量。因此,如何有效监测和评估冷冻过程中纺锤体的变化,成为纺锤体卵冷冻研究的重要课题。纺锤体实时成像技术的出现,为这一问题的解决提供了可能。纺锤体实时成像技术主要利用高分辨率显微镜结合荧光标记技术,对卵母细胞内的纺锤体进行实时、动态的观察和记录。常用的荧光标记方法包括使用绿色荧光蛋白(GFP)标记微管蛋白,以及利用特定抗体对纺锤体相关蛋白进行染色。通过这些方法,研究者可以清晰地观察到纺锤体的形态、位置、动态变化等信息,从而准确评估冷冻过程中纺锤体的稳定性和完整性。北京核移植纺锤体胚胎发育