商机详情 -
连云港药理学实用膜片钳技术
膜片钳技术基本原理与特点:膜片钳技术本质上也属于电压钳范畴,两者的区别关键在于:①膜电位固定的方法不同;②电位固定的细胞膜面积不同,进而所研究的离子通道数目不同。电压钳技术主要是通过保持细胞跨膜电位不变,并迅速控制其数值,以观察在不同膜电位条件下膜电流情况。因此只能用来研究整个细胞膜或一大块细胞膜上所有离子通道活动。目前电压钳主要用于巨大细胞的全性能电流的研究,特别在分子克隆的卵母细胞表达电流的鉴定中发挥着其他技术不能替代的作用。内面向外式膜片细胞内外和电极内的溶液均可调控。连云港药理学实用膜片钳技术
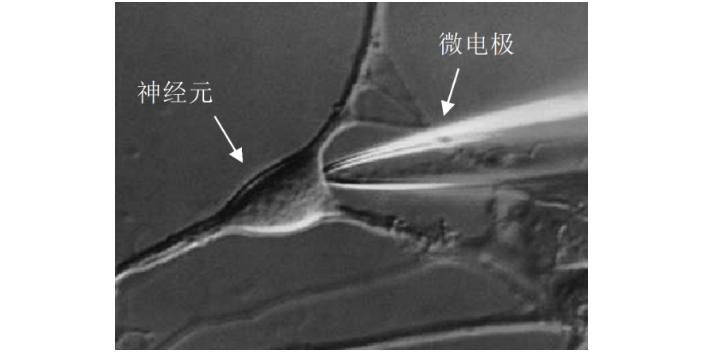
膜片钳技术在通道研究中的重要作用:利用膜片钳技术还可以用于药物在其靶受体上作用位点的分析。如神经元烟碱受体为配体门控性离子通道,膜片钳全细胞记录技术通过记录烟碱诱发电流,可直观地反映出神经元烟碱受体活动的全过程,包括受体与其激动剂和拮抗剂的亲和力,离子通道开放、关闭的动力学特征及受体的失敏等活动。使用膜片钳全细胞记录技术观察拮抗剂对烟碱受体激动剂量效曲线的影响,来确定其作用的动力学特征。然后根据分析拮抗剂对受体失敏的影响,拮抗剂的作用是否有电压依赖性、使用依赖性等特点,可从功能上区分拮抗剂在烟碱受体上的不同作用位点,即判断拮抗剂是作用在受体的激动剂识别位点,离子通道抑或是其它的变构位点上。苏州药理学膜片钳技术技术用膜片钳技术可以直接观察和分辨单离子通道电流及其开闭时程。
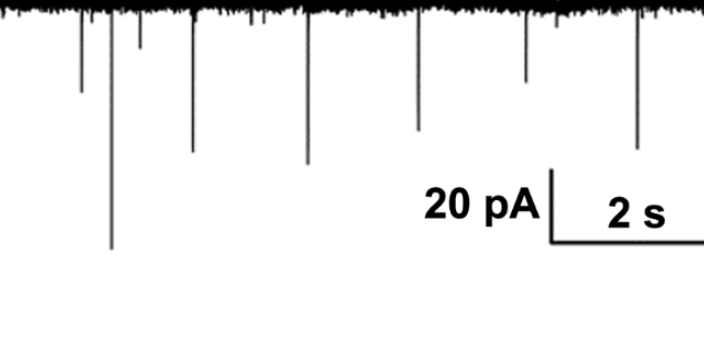
全细胞膜片钳模式下有电压钳记录和电流钳记录两种。电压钳记录的原理与电压钳技术相似,但有所不同:首先,全细胞电压钳记录只使用单根电极,但在电学效果上同时实现了电压钳制和电流记录。其次,电压钳记录的电极不细胞,对细胞造成的损伤较小,因而能用于小细胞如神经元的研究。电流钳记录则是通过钳制电极电流来测量膜电位。电流钳在本质上也是电压钳位,它将差分放大器的输出电流与指令电流相比较,然后将这个差动输出施加到放大器前级的倒相端,通过高速反馈使得同相端的电压与其相等,无论电极电流是否为零,都能从输出电压得到膜电位的准确数值。
膜片钳技术是通过微玻管电极(膜片电极或膜片吸管)接触细胞膜,用千兆欧姆以上的阻抗使之封接,在电学上分隔和电极尖开口处相接的细胞膜的小区域(膜片)以及其周围,在此基础上固定点位,对这膜片上的离子通道的离子电流(pA级)进行监测记录的方法。测量回路的中心部分是使用场效应管运算放大器构成的I-V转换器。当场效应管运算放大器的正负输入端子是等电位,向正输入端子施加指令电位时,因为短路负端子以及膜片都可等电位地达到钳制的作用,字膜片微电极与默片之间形成10GΩ以上封接时,其间达到Z小的分流电流。膜片钳的数据如何处理:通过渗透很快改变胞浆成分并达到平衡,该手段在全细胞记录中广泛应用。
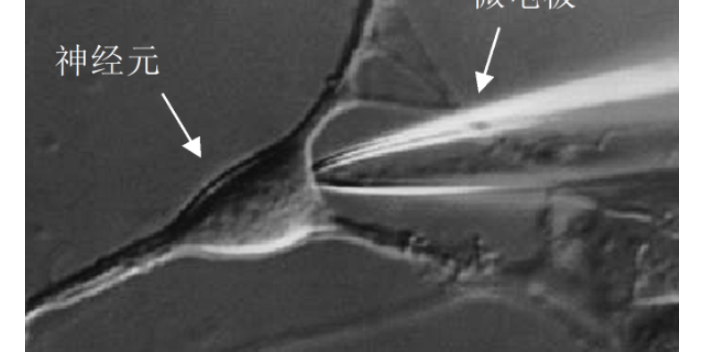
膜片钳操作实验:标本制备根据研究目的的不同,可采用不同的细胞组织,如心肌细胞、平滑肌细胞、细胞等,现在几乎可对各种细胞进行膜片钳的研究。对所采用的细胞,必须满足实验要求,一般多采用酶解分离法,也可采用细胞培养法;另外,由于与分子生物学技术的结合,现在也运用分子克隆技术表达不同的离子通道,如利用非洲爪蟾卵母细胞表达外源性基因等。电极在实验前要灌注电极液,由于电极较细,因此在充灌前,电极内液要用0.2 μm的滤膜进行过滤。一般电极充灌可分灌尖(tipfilling)和后充两步灌尖时将电极浸入内液中5s即可。膜片钳技术是电生理记录的常用手段,目前在科学研究中使用越来越普遍。连云港药理学实用膜片钳技术
膜片钳技术的建立,对生物学科学特别是神经科学是一资有重大意义的变革。连云港药理学实用膜片钳技术
膜片钳技术是在电压钳技术基础上发展起来的,电压钳是利用负反馈技术将膜电位在空间和时间上固定于某一测定值,以研究动作电位产生过程中膜的离子通透性与膜电位之间的依从关系。但电压钳只能研究一个细胞上众多通道的综合活动规律,而无法反映单个通道的活动特点,同时通过细胞内微电极引导记录的离子通道电流其背景噪声太大。膜片钳使用的基本方法是,把经过加热抛光的玻璃微电极在液压推进器的操纵下,与清洁处理过的细胞膜形成高阻抗封接,导致电极内膜片与电极外的膜在电学上和化学上隔离起来。连云港药理学实用膜片钳技术