商机详情 -
苏州干细胞定向诱导分化服务平台
展望未来,细胞生物学技术将取得更大突破。随着基因编辑技术如 CRISPR - Cas9 的不断完善,细胞基因组的精细修饰将更加高效和准确,为基因医疗和疾病模型构建带来新机遇。单细胞多组学技术的发展,将使我们能够在单细胞水平多方面解析细胞的基因表达、表观遗传等信息,深入了解细胞的异质性。类部位技术的兴起,有望构建更接近体内生理状态的细胞模型,用于药物研发和疾病研究。同时,细胞生物学技术与人工智能、大数据的结合,将加速数据的分析和处理,推动生命科学研究向更高水平迈进。细胞生物学技术服务采用 RNA 干扰技术,沉默细胞内特定基因表达,研究基因功能。苏州干细胞定向诱导分化服务平台
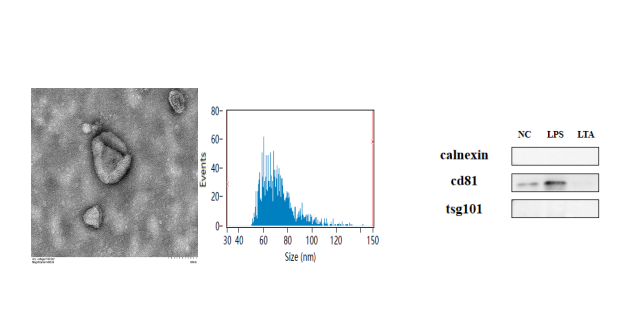
细胞自噬是细胞维持内环境稳态的重要 “自我清理” 机制,其研究技术不断创新。透射电子显微镜作为 “金标准”,凭借超高分辨率捕捉到自噬体、自噬溶酶体的双层膜结构,直观证实自噬的发生。基于荧光蛋白标记的自噬标记物,如 LC3,通过荧光显微镜实时监测自噬流的动态过程,判断细胞自噬活性。在神经退行性疾病领域,研究发现自噬功能障碍导致异常蛋白聚集,利用自噬诱导剂激发自噬,观察细胞内病理蛋白清理情况,为疾病医疗寻找新靶点,有望延缓病情进展,开启细胞内环境净化新途径。简单稳转株细胞构建服务细胞生物学技术服务通过单细胞功能分析技术,深入研究单个细胞的生物学特性。
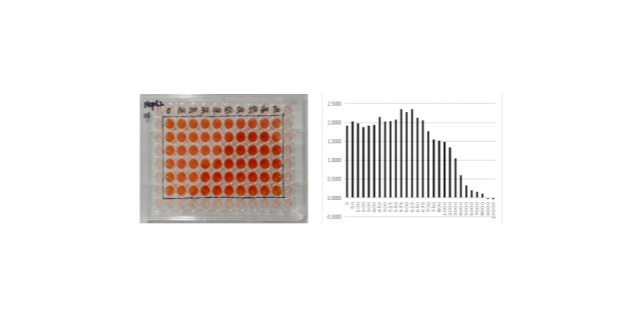
以细胞培养为例,首先要获取合适的细胞来源,如从组织中分离原代细胞或使用已建立的细胞系。对获取的细胞进行复苏(若为冻存细胞),将其接种到含有适宜培养液的培养器皿中,置于培养箱中培养。培养过程中,需定期观察细胞的生长状态,根据细胞密度进行传代培养。当需要进行细胞转染时,先将外源核酸与转染试剂混合形成复合物,然后加入到培养的细胞中,孵育一定时间,使复合物进入细胞。对于荧光标记实验,先将荧光探针与目标分子结合,再将其加入细胞培养液中,待标记完成后,在荧光显微镜下进行观察和成像。每个实验流程都需严格遵守无菌操作原则,确保实验结果的准确性和可靠性。
单细胞分析技术能揭示细胞的异质性。单细胞测序技术可对单个细胞的基因组、转录组、表观基因组等进行测序分析。以单细胞转录组测序为例,首先将单个细胞分离出来,提取 RNA 并逆转录为 cDNA,然后进行 PCR 扩增,构建测序文库,通过高通量测序,可获得每个细胞的基因表达谱,发现不同细胞亚群的特征基因。单细胞蛋白质组学则利用质谱技术,分析单个细胞内蛋白质的表达和修饰情况。此外,微流控技术在单细胞分析中也有广泛应用,通过微流控芯片,可实现单细胞的捕获、操控、反应和分析,为单细胞水平的研究提供了高效、精细的平台。细胞生物学技术服务提供细胞外泌体分离与鉴定服务,探索细胞间通讯新途径。

细胞生物学技术服务涵盖多种技术,以细胞培养为例,其原理是将细胞从生物体中取出,在体外模拟体内的生理环境,提供适宜的温度、湿度、营养物质等条件,使细胞能够生存、生长、繁殖。如在培养哺乳动物细胞时,需提供含有人工合成培养基、血清、抑生素等成分的培养液。而细胞转染技术,是通过物理、化学或生物方法,将外源核酸(如 DNA、RNA)导入细胞内。例如电穿孔法,利用高压电脉冲在细胞膜上形成瞬间小孔,使核酸分子进入细胞。荧光标记技术则是利用荧光基团与细胞内特定分子结合,在荧光显微镜下观察细胞结构和分子动态。这些技术为深入研究细胞的结构、功能、代谢等提供了基础。细胞生物学技术服务涵盖细胞培养、转染等,满足科研人员多样化实验需求。苏州干细胞定向诱导分化服务平台
细胞生物学技术服务以标准化流程,进行细胞毒性检测,保障药物安全性。苏州干细胞定向诱导分化服务平台
细胞生物学技术在众多领域发挥关键作用。在生物制药领域,通过细胞培养技术生产重组蛋白药物,如胰岛素、干扰素等,利用细胞作为 “工厂” 高效合成药用蛋白。在瘤子研究中,借助细胞转染技术将致病基因或抑病基因导入细胞,构建肿瘤细胞模型,研究瘤子发长头发展机制,筛选抗病药物。在再生医学方面,运用干细胞培养和分化技术,诱导干细胞分化为特定组织细胞,用于修复受损组织和部位。在免疫学研究中,利用细胞分选技术分离不同类型的免疫细胞,研究免疫反应机制,开发免疫治疗方法。在农业领域,细胞融合技术用于培育优良作物品种,提高农作物的产量和品质。苏州干细胞定向诱导分化服务平台