商机详情 -
海南近红外二区X射线-荧光双模态成像系统执行标准
双模态数据的病理关联分析:影像与组织学的定量整合系统支持双模态影像与组织病理学数据的配准分析,在骨**研究中,将X射线的骨破坏区域、荧光的肿瘤细胞分布与病理切片的HE染色结果叠加,可量化影像指标与病理分级的一致性(如G3级**的荧光强度较G1级高3倍)。这种整合分析使影像诊断的准确率从75%提升至92%,并能发现传统病理难以量化的空间分布特征,如肿瘤细胞沿骨小梁间隙的浸润模式。 X射线—荧光双模态成像系统支持骨靶向纳米药物的分布评估,X射线定位骨骼,荧光追踪药物蓄积。X射线—荧光双模态成像系统的剂量累积监控功能,自动优化扫描参数以降低动物辐射暴露。海南近红外二区X射线-荧光双模态成像系统执行标准
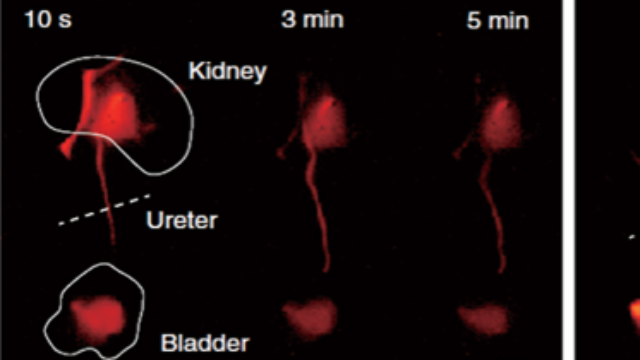
双模态影像的实时传输与远程诊断:跨地域科研协作系统支持双模态影像的实时加密传输,科研中心可远程指导分中心的成像操作,如调整X射线角度或荧光探针激发参数。在跨国骨肿块研究中,该功能实现多地域实验数据的同步分析,例如德国实验室通过X射线确认骨破坏类型,美国团队基于荧光标记的PD-L1表达制定免疫治疗方案,数据传输延迟<200ms,确保跨地域协作的时效性。这种远程诊断模式将多中心研究的筹备周期从6个月缩短至2个月,大幅提升科研效率。北京小动物X射线-荧光双模态成像系统咨询问价X射线—荧光双模态成像系统支持术中实时导航,通过X射线定位骨肿块与荧光标记边界。
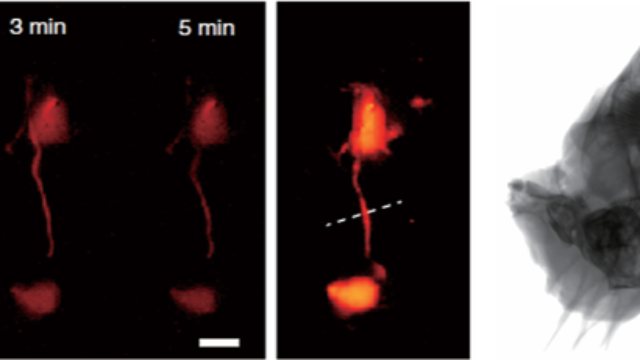
轻量化便携设计:床边与术中的灵活应用针对临床转化需求,双模态系统开发了便携式版本(主机重量<10kg),X射线模块采用平板探测器(10×10cm),荧光通道集成光纤阵列探头,可在动物手术室或病床边实现即时成像。在骨科急症中,该设备可快速评估骨折类型(X射线)与周围组织损伤(荧光标记的炎症因子),为急诊手术方案提供影像支持,从成像到报告的全流程耗时<15分钟,较传统影像学检查效率提升50%。该系统在骨发育研究中通过X射线追踪骨骼生长板变化,荧光标记生长因子表达动态。
骨微损伤的双模态量化:早期骨质疏松的预警指标系统通过高分辨X射线(2μm分辨率)识别骨小梁微裂纹(长度>50μm),配合荧光标记的骨细胞凋亡(AnnexinV探针),在骨质疏松模型中发现微裂纹区域的骨细胞凋亡率较正常区域高3倍,且X射线微裂纹数量与荧光凋亡信号的相关性达0.92。该技术可在骨密度下降前6个月检测到微损伤,为骨质疏松的早期预警提供结构-分子双重指标,较传统DXA检测提前发现风险。 X射线—荧光双模态成像系统的多参数分析模块,量化骨体积分数与荧光信号强度的相关性。双模态系统在骨转移研究中通过X射线识别溶骨病灶,荧光标记肿瘤细胞活性。
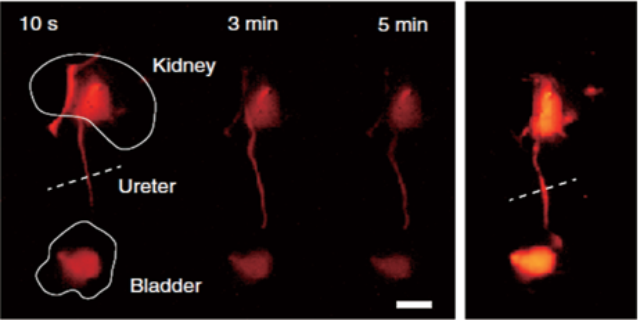
自适应剂量调节:辐射安全与成像效率的平衡双模态系统的智能剂量算法可根据样本厚度自动调节X射线参数(10-50kV),在小鼠全身骨成像中将单次辐射剂量控制在0.5mGy以下(相当于胸部CT的1/10),同时通过近红外二区荧光(1000-1700nm)提升分子信号的信噪比(达8:1)。在长期纵向研究中,该技术可实现每周2次的重复扫描,追踪骨转移*的进展与***响应,较传统高剂量X射线方案减少动物辐射损伤风险达70%。双模态系统的辐射防护铅舱设计,将操作人员暴露剂量控制在安全阈值以下。低温制冷的荧光相机与脉冲式X射线源协同,使系统实现快速双模态数据采集(<10秒/次)。海南近红外二区X射线-荧光双模态成像系统执行标准
X射线—荧光双模态成像系统的AI模型预测功能,基于双模态数据预测骨肿块的转移风险。海南近红外二区X射线-荧光双模态成像系统执行标准
低剂量动态扫描:纵向研究的辐射安全方案针对需要长期观察的骨发育研究,系统采用“低剂量脉冲扫描”模式,单次X射线剂量<0.1mGy,配合高灵敏度荧光检测,可每周追踪小鼠骨骼生长板的变化(X射线量化软骨厚度)与生长因子表达(荧光标记IGF-1)。在侏儒症模型中,双模态成像显示生长板软骨厚度每周减少15μm,同时IGF-1荧光强度下降20%,这种无损动态监测为骨骼发育障碍的机制研究提供连续数据,避免传统处死取材导致的个体差异误差。 X射线—荧光双模态成像系统的剂量累积监控功能,自动优化扫描参数以降低动物辐射暴露。海南近红外二区X射线-荧光双模态成像系统执行标准