商机详情 -
中国台湾X射线-荧光双模态成像系统哪家强
双模态成像的未来技术升级:AI+多模态的智能融合系统预留AI算法接口与多模态扩展端口,未来可集成机器学习模型(如基于Transformer的骨疾病预测网络)与质谱成像(MALDI),实现“X射线结构-AI预测-荧光验证-质谱代谢”的四维分析。在概念验证实验中,AI模型基于双模态数据预测骨肿块的转移风险(AUC=0.95),并通过质谱成像验证预测区域的代谢异常(如脂质代谢通路打开),为骨骼疾病的精细医学研究开辟“影像-分子-代谢”的多维研究范式。X射线—荧光双模态成像系统的参数化报告生成功能,自动输出骨结构与分子标记的量化指标。中国台湾X射线-荧光双模态成像系统哪家强
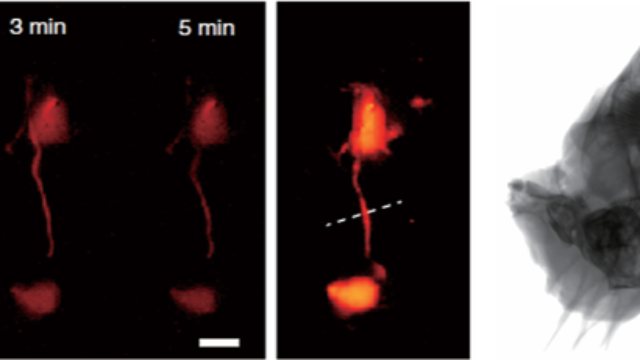
双模态成像的运动员骨骼健康监测:运动医学的精细防护针对职业运动员,便携式双模态设备可快速评估应力性骨折风险:X射线量化骨皮质增厚程度(如增厚>0.2mm),荧光标记的骨细胞机械应力响应(YAP/TAZ探针)显示应力集中区域(荧光强度高1.8倍)。该技术可在临床症状出现前2周发现潜在损伤,为运动员的训练调整与康复计划提供影像依据,在篮球运动员队列研究中使应力性骨折发生率降低40%。 集成AI辅助诊断的双模态系统,自动检测X射线骨结构异常并关联荧光标记的病理信号。小动物X射线-荧光双模态成像系统对比兼容小动物与大动物模型的双模态系统,为骨疾病转化研究提供跨物种成像解决方案。
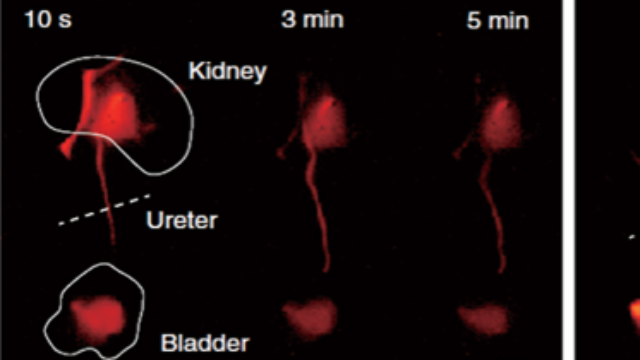
X射线—荧光双模态成像系统:骨骼与分子的精细对话该系统创新性融合X射线的高分辨率解剖成像(5μm微焦斑)与近红外荧光的分子标记能力,在骨肿块研究中可同步呈现溶骨***灶的X射线灰度变化(骨皮质破坏程度)与荧光探针标记的肿瘤细胞活性(如Ki67蛋白表达)。通过智能配准算法,自动将X射线骨结构与荧光信号叠加,形成“解剖-分子”关联图谱,例如在小鼠股骨肿块模型中,可量化肿块体积与荧光强度的相关性(R²=0.91),较单一模态更精细评估肿块进展。
双模态成像的考古学应用:古生物骨骼的非破坏性研究针对考古骨骼样本,系统通过低剂量X射线(<0.01mGy)解析化石骨微结构(如哈弗斯系统形态),荧光光谱分析(1000-1700nm)检测有机残留物(如胶原蛋白荧光),在古人类化石研究中发现:尼安德特人化石的骨小梁连接度较现代人类高15%,且荧光光谱显示胶原蛋白保存度达30%。这种非破坏性双模态技术为考古学研究提供分子与结构的双重证据,避免传统切片对珍贵化石的破坏。该系统在骨关节炎研究中通过X射线评估软骨下骨变化,荧光标记炎症因子表达。动态时序采集功能让X射线—荧光成像系统记录骨折修复中骨痂矿化与血管生成的时空关联。
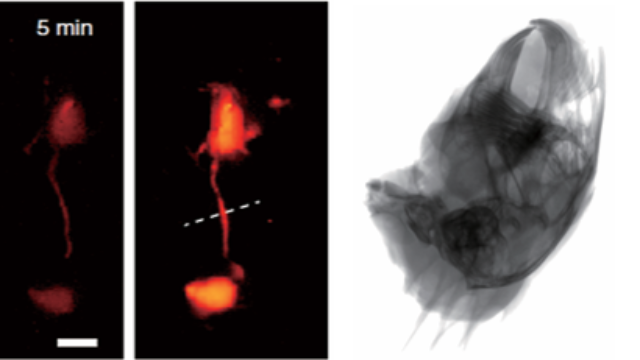
AI辅助诊断:双模态数据的智能分析内置的卷积神经网络模型可自动检测X射线中的骨结构异常(如溶骨、成骨病灶),并关联荧光通道的分子标记强度。在骨转移*筛查中,AI算法对X射线病灶的检出灵敏度达98%,且能根据荧光信号强度预测肿块恶性程度(与病理分级的一致性达91%)。该功能将传统需要4小时的影像分析缩短至20分钟,尤其适合大规模队列研究中的骨疾病早期筛查。实时图像融合算法让X射线—荧光成像系统在骨科微创手术中同步显示骨结构与肿块边界。在骨扩散研究中,X射线—荧光成像系统识别骨皮质破坏,荧光标记细菌生物膜分布。上海成像系统X射线-荧光双模态成像系统咨询问价
X射线—荧光双模态成像系统的无线数据传输功能,支持手术间与实验室的实时影像共享。中国台湾X射线-荧光双模态成像系统哪家强
双模态引导的干细胞移植:骨骼再生的精细调控在骨缺损修复中,X射线定位缺损区域(如直径5mm的颅骨缺损),荧光标记间充质干细胞(GFP+)的移植轨迹,系统可量化细胞在缺损区的聚集效率(24小时达85%)及成骨分化程度(OCN荧光强度随时间上升2.1倍)。结合X射线的新骨矿化评估(术后4周骨密度达正常的60%),该技术为干细胞疗法的剂量优化与移植路径设计提供可视化依据,使骨再生效率提升40%。 低温制冷的荧光相机与脉冲式X射线源协同,使系统实现快速双模态数据采集(<10秒/次)。中国台湾X射线-荧光双模态成像系统哪家强