商机详情 -
山东全光谱近红外二区显微成像系统哪家强
光声-荧光双模态:结构与功能的协同解析近红外二区显微成像系统创新性集成光声与荧光双模态。光声模块通过1550nm激光激发血红蛋白,以50μm分辨率重建肿块血管网络,同步量化血氧分压(pO2)分布;荧光模块则利用1200nm波段探针标记肿瘤细胞表面受体,实现分子层面的精细定位。在抗血管生成药物筛选实验中,该系统可实时观察药物干预后血管密度(光声)与受体表达(荧光)的协同变化,较单一模态实验效率提升2倍,数据相关性达0.91。基于光纤阵列的显微探头设计,让近红外二区成像系统实现深部组织的微创式观测。山东全光谱近红外二区显微成像系统哪家强
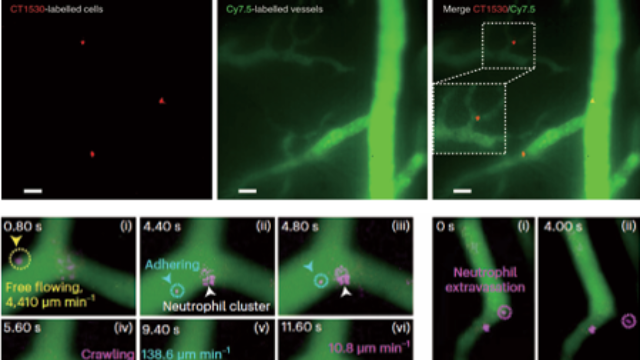
子宫黏膜成像:生殖周期的动态观察针对生殖医学研究,系统通过近红外二区荧光标记的雌***受体(1200nm探针),追踪子宫黏膜的周期性变化。在动情周期模型中,可观察到受体在增殖期的核转位效率(70%)明显高于分泌期(30%),并量化黏膜血管的生成密度(增殖期较分泌期高2倍)。该技术与子宫内膜厚度测量(超声)的相关性达0.88,且能提供分子层面的功能信息,如发现雌***受体阳性细胞的分布与胚胎着床窗口的空间对应关系,为辅助生殖技术的内膜准备方案优化提供新依据。河北荧光近红外二区显微成像系统维保搭载InGaAs深度制冷相机,该系统在近红外二区实现单光子级检测灵敏度,捕捉微弱生物信号。
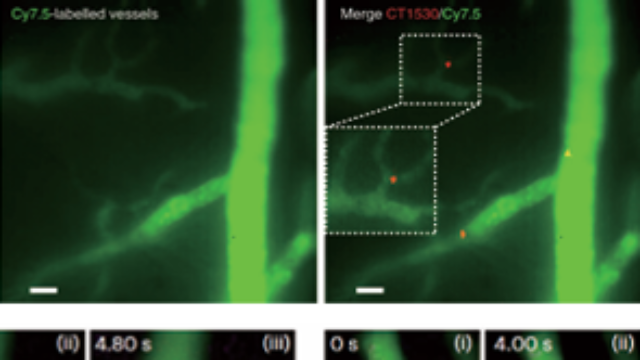
前列腺*成像:早期诊断与转移的精细评估近红外二区显微成像系统通过1100nm荧光标记的前列腺特异性膜抗原(PSMA)探针,实现前列腺*的高灵敏度检测。在小鼠模型中,可识别直径0.5mm的原位*灶(信噪比8:1),并通过光声成像评估肿块内的微血管密度(较正常前列腺高2.3倍)。系统支持淋巴结转移的早期检测,如发现PSMA阳性的微转移灶(直径<0.2mm)在常规病理检测中易被漏诊,为前列腺*的分期与治疗方案选择提供精细影像支持,较传统MRI的灵敏度提升40%。
近红外二区成像:突破组织光学壁垒的科研利器近红外二区(NIR-II,1000-1700nm)显微成像系统凭借生物组织对该波段光的低散射、低自发荧光特性,实现10mm深度内的高分辨***成像。其搭载的InGaAs深度制冷相机(-90℃温控)将暗电流抑制至0.01e⁻/pixel/sec以下,配合飞秒激光光源(脉宽<100fs),在脑血管成像中可清晰分辨直径5μm的***,且穿透颅骨时信号衰减不足30%。相较传统可见光成像,该系统在肿块转移研究中能提前48小时发现直径0.3mm的肺转移灶,为早期诊断提供关键影像支撑。近红外二区显微成像系统的温度敏感荧光探针适配功能,监测组织微环境温度变化。

肺部气体交换成像:呼吸功能的可视化评估结合近红外二区荧光微球(1050nm)灌注与光声成像,系统量化肺部的气体交换效率。在慢性阻塞性肺疾病(COPD)模型中,可观察到肺泡***床的破坏程度(血管密度降低35%),并通过微球滞留时间评估气体交换面积(较正常减少40%)。该技术与肺功能测试(FEV1/FVC)的相关性达0.87,为肺部疾病的病理机制研究提供结构-功能一体化的影像证据,且无需放射性示踪剂。该显微成像系统在近红外二区量化纳米药物在肿块组织的蓄积效率与分布动力学。该显微成像系统在近红外二区量化纳米药物在肿块组织的蓄积效率与分布动力学。河北荧光近红外二区显微成像系统维保
近红外二区显微成像系统的AI辅助诊断模块,自动识别病变区域并生成量化分析报告。山东全光谱近红外二区显微成像系统哪家强
微创光纤成像:深部组织的原位观测基于光纤阵列设计的显微探头(直径0.5mm),使近红外二区成像系统可通过颅骨钻孔(直径1mm)实现小鼠脑深部核团(如黑质、纹状体)的长期观测。在帕金森病模型中,该探头配合1200nm荧光探针标记多巴胺能神经元,连续7天追踪细胞凋亡过程,信号稳定性误差<5%。相较传统开颅成像,术后扩散率降低80%,动物存活率提升至95%。双模态光声-荧光成像模块集成,为近红外二区显微成像系统构建结构与功能的双重解析能力。山东全光谱近红外二区显微成像系统哪家强