商机详情 -
浙江荧光近红外二区显微成像系统维保
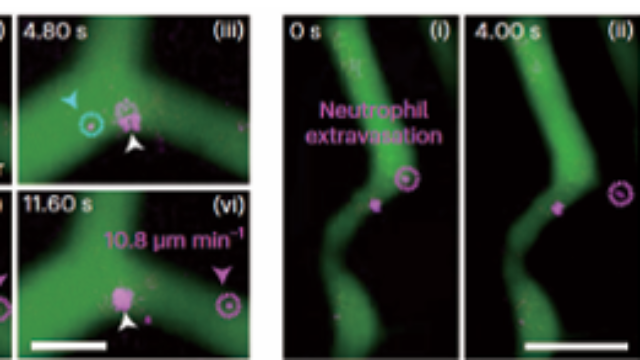
肠道屏障功能成像:炎症性肠病的病理机制解析利用近红外二区荧光标记的紧密连接蛋白探针(1150nm),系统实时监测肠道屏障的完整性。在炎症性肠病模型中,可观察到肠上皮细胞间紧密连接的破坏程度(荧光强度下降50%),并通过跨上皮电阻(TEER)模拟计算屏障通透性(与传统TEER检测的相关性达0.89)。配合免疫荧光成像标记的炎症细胞,可构建“屏障损伤-炎症浸润”的动态关联模型,如发现中性粒细胞浸润区域的紧密连接破坏程度较非浸润区高3倍,为肠道炎症的靶向医治提供新靶点。该显微成像系统通过近红外二区光谱分析,量化组织的脂质代谢状态。浙江荧光近红外二区显微成像系统维保
光声断层成像:深部肿块的三维血管建模系统的光声断层成像(PAT)模块以500nm空间分辨率重建肿块的三维血管网络,在10mm深度内可识别直径20μm的血管分支。在抗血管生成药物实验中,PAT可量化肿块血管的分形维数(用药后从1.7降至1.3)、血管表面积密度(从280mm²/mm³降至150mm²/mm³),这些结构参数与肿块体积抑制率(r=0.91)高度相关。配合荧光成像标记的肿瘤细胞,可构建“血管供养-肿块生长”的三维关联模型。基于微机电系统(MEMS)的快速扫描镜,让近红外二区显微成像系统实现大范围动态观测。浙江荧光近红外二区显微成像系统维保配备高数值孔径物镜的近红外二区系统,提升微弱荧光信号的收集效率。
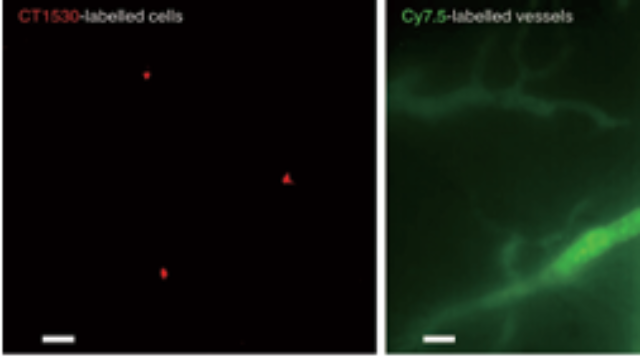
胎盘-胎儿互作成像:妊娠疾病的机制研究针对妊娠研究,系统通过近红外二区荧光成像观察胎盘血管网络与胎儿发育的关联。在子痫前期模型中,可量化胎盘绒毛间隙的血流速度(降低28%)与血管分支数量(减少30%),并通过探针标记的营养转运蛋白评估胎盘屏障功能(转运效率下降40%)。该技术与胎儿体重增长(r=0.93)直接关联,为妊娠并发症的病理机制研究提供可视化工具,且无需侵入性操作,保障母胎安全。基于深度学习的图像降噪算法,提升近红外二区显微成像的信噪比与分辨率。
骨组织微结构成像:从发育到修复的全程解析系统结合X-ray微CT与近红外二区荧光成像,构建骨组织的结构-功能联合分析。在骨质疏松模型中,X-ray模块量化骨小梁厚度(误差<5%),荧光模块通过1150nm标记的成骨细胞特异性探针,显示新骨形成区域,两者配准后可计算骨形成速率(BFR)与骨吸收表面(ES/BS)的动态平衡。该技术在抗骨质疏松药物筛选中,可将药效评估周期从8周缩短至4周,且数据重复性CV<8%。近红外二区显微成像系统的高通量载物台,支持多样本并行成像提升实验效率。采用光纤光谱仪的近红外二区系统,实时分析生物分子的振动光谱特征。

近红外二区成像:突破组织光学壁垒的科研利器近红外二区(NIR-II,1000-1700nm)显微成像系统凭借生物组织对该波段光的低散射、低自发荧光特性,实现10mm深度内的高分辨***成像。其搭载的InGaAs深度制冷相机(-90℃温控)将暗电流抑制至0.01e⁻/pixel/sec以下,配合飞秒激光光源(脉宽<100fs),在脑血管成像中可清晰分辨直径5μm的***,且穿透颅骨时信号衰减不足30%。相较传统可见光成像,该系统在肿块转移研究中能提前48小时发现直径0.3mm的肺转移灶,为早期诊断提供关键影像支撑。近红外二区显微成像系统以1000-1700nm波长突破组织散射极限,实现深层生物结构的高分辨可视化。浙江荧光近红外二区显微成像系统维保
近红外二区显微成像系统的激光功率智能调节功能,避免强光对样本造成光损伤。浙江荧光近红外二区显微成像系统维保
免疫细胞动态监测:从迁移到活化的全程记录利用CFSE标记的T细胞(1050nm荧光),系统在近红外二区追踪免疫细胞在肿块组织的迁移轨迹。在CAR-T医治实验中,可观察到CAR-T细胞在肿块边缘的“爬行”运动(速度12μm/min)及与肿瘤细胞的动态接触(平均作用时间3分钟),同步通过钙信号成像评估T细胞活化程度。这些动态数据与肿块缩小率(R²=0.86)直接关联,为免疫细胞医治的疗效预测提供新范式。 双光子激发技术结合近红外二区探测,为系统带来亚细胞级分辨率的成像能力。浙江荧光近红外二区显微成像系统维保