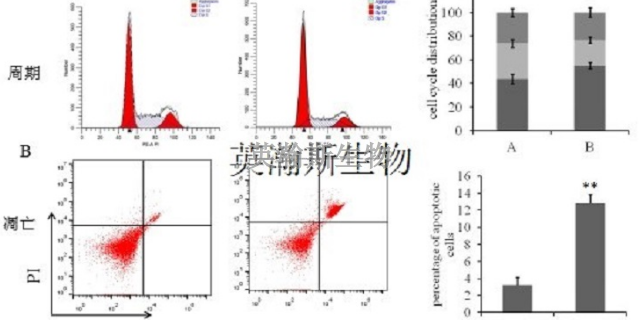
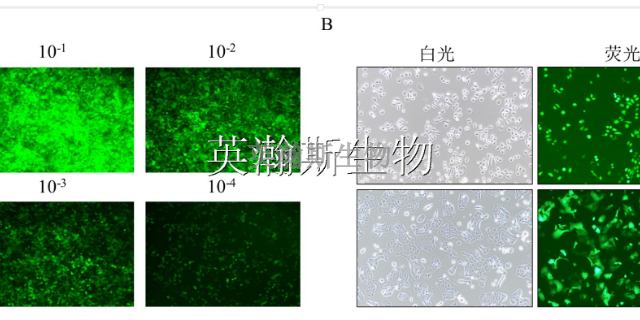
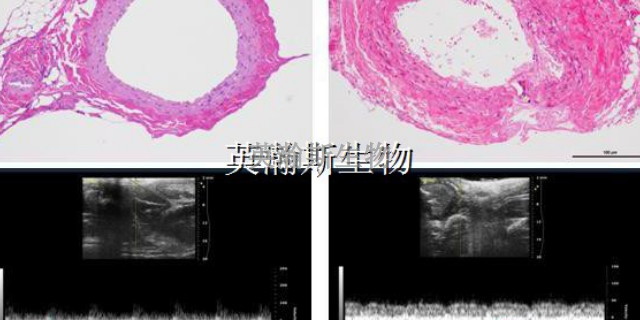
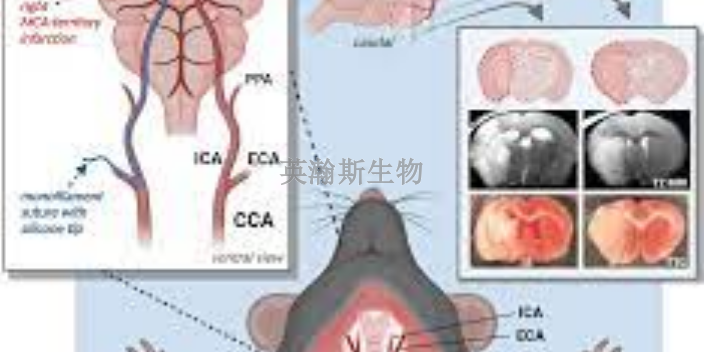
-
 南京市生物外包公司是哪家
发布时间:2024.03.05
南京市生物外包公司是哪家
发布时间:2024.03.05
生物外包公司主要从事生物实验,生物实验是生命科学的基础,它可以帮助我们了解生命的起源、结构、功能、发展和演化,以及与环境的相互作用。生物实验可以分为基础生物实验和应用生物实验两大类。基础生物实验是指为...
-
 甘肃哪里有生物外包公司名字
发布时间:2024.03.05
甘肃哪里有生物外包公司名字
发布时间:2024.03.05
生物外包公司生物实验是一种创新性的研究方法,它需要不断地提出新的问题,设计新的方案,发现新的现象,解释新的规律,创造新的知识。为了进行有创意的生物实验,我们需要具备以下几方面的素质:(1)好奇心:能够...
-
 南京专门做生物外包公司有哪些
发布时间:2024.03.04
南京专门做生物外包公司有哪些
发布时间:2024.03.04
生物外包公司通常会将需要使用动物进行的科学研究或试验交给具有相应资质和经验的第三方机构或公司来完成,而不是自己在实验室内进行。动物实验外包可以节省时间、成本、人力和设备,提高实验的效率和质量,避免...
-
 甘肃专业的生物外包公司电话多少
发布时间:2024.03.03
甘肃专业的生物外包公司电话多少
发布时间:2024.03.03
生物外包公司主要从事生物实验是科学研究,通过实验可以验证假设、发现新的知识,并推动生物学领域的进步。生物学家们使用各种实验方法来研究生物体的结构、功能和相互作用。在生物实验中,动物模型经常被用来研究疾...
-
 靠谱的生物外包公司电话多少
发布时间:2024.03.03
靠谱的生物外包公司电话多少
发布时间:2024.03.03
生物外包公司主要从事生物实验是科学研究,通过实验可以验证假设、发现新的知识,并推动生物学领域的进步。生物学家们使用各种实验方法来研究生物体的结构、功能和相互作用。在生物实验中,动物模型经常被用来研究疾...
-
 南京哪里有生物外包公司有哪些
发布时间:2024.03.02
南京哪里有生物外包公司有哪些
发布时间:2024.03.02
选择生物实验外包公司要有场地、有设备、有技术员的公司。既然选择实验外包,那么我们关注的就是数据真实性问题,试问一个连实验室、实验设备和实验员都没有的公司如何做到给你一个真实可靠地实验数据呢?有些公...
-
 广西哪里有生物外包公司
发布时间:2024.03.01
广西哪里有生物外包公司
发布时间:2024.03.01
生物外包公司的工作是生物实验是一种多学科交叉的研究方法,它涉及到数学、物理、化学、计算机等多个领域的知识和技能。为了进行高水平的生物实验,我们需要掌握以下几方面的能力:(1)数学能力:能够运用数学公式...
-
 河南专门做生物外包公司是哪家
发布时间:2024.02.29
河南专门做生物外包公司是哪家
发布时间:2024.02.29
生物外包公司主要从事生物实验,生物实验是生命科学的基础,它可以帮助我们了解生命的起源、结构、功能、发展和演化,以及与环境的相互作用。生物实验可以分为基础生物实验和应用生物实验两大类。基础生物实验是指为...
-
 青海比较好的生物外包公司电话多少
发布时间:2024.02.28
青海比较好的生物外包公司电话多少
发布时间:2024.02.28
生物实验外包公司 实验外包即将实验外包于科研机构之外的第三方实验室,已经成为发展趋势。第三方实验室不仅实验设备先进,可操作实验的规模和种类也是多种多样,国家层面也出台政策推动科研单位与企业利用资源优势...
-
 江苏靠谱的生物外包公司有哪些
发布时间:2024.02.27
江苏靠谱的生物外包公司有哪些
发布时间:2024.02.27
生物外包公司可以做生物实验也包括植物生物学领域,研究植物的生长、发育和生态系统。这些实验对于农业、环境保护和食品产业都具有重要意义。生物实验不仅限于实验室,还包括野外研究和生态学研究。科学家们通过观察...
-
 广西靠谱的生物外包公司名字
发布时间:2024.02.27
广西靠谱的生物外包公司名字
发布时间:2024.02.27
选择生物实验外包公司注意不要贪图价格低的公司。实验外包都是有一个市场价格,靠谱公司的价格都不算贵,但也不会太便宜,毕竟实验耗材、实验试剂、实验设备还有人工费用都是需要成本的。如果报价比较低的话,就需要...
-
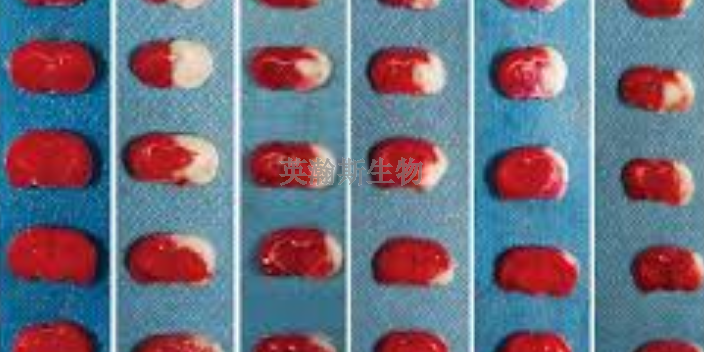
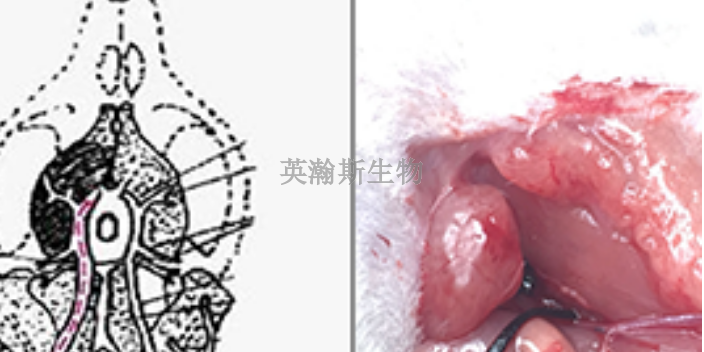
 四川小鼠脑缺血再灌注模型价格
发布时间:2024.02.26
四川小鼠脑缺血再灌注模型价格
发布时间:2024.02.26
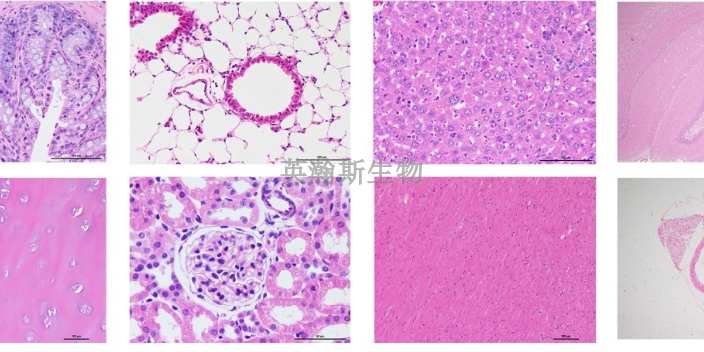
脑缺血再灌注模型的病理学评估主要有两种方法,即TTC染色法和HE染色法。TTC染色法是利用2,3,5-三苯基四唑(TTC)对***组织进行染色,TTC可以被正常组织中的脱氢酶还原成红色产物,而缺血...
-
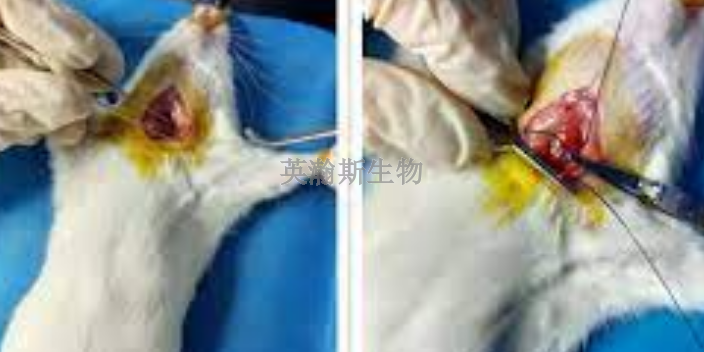
 辽宁脑缺血再灌注模型造模
发布时间:2024.02.25
辽宁脑缺血再灌注模型造模
发布时间:2024.02.25
大鼠脑缺血再灌注造模是研究脑缺血再灌注损伤的常用实验模型之一。该模型通过暂时阻断大鼠脑部血液供应,并在一定时间后再恢复血流,模拟脑缺血再灌注的过程。这种模型可以帮助研究人员深入了解脑缺血再灌注损伤的发...
-
 靠谱的脑缺血再灌注模型
发布时间:2024.02.25
靠谱的脑缺血再灌注模型
发布时间:2024.02.25
脑缺血再灌注造模的应用非常的***,特别是在研究中风和其他脑血管疾病方面。通过模拟缺血再灌注的过程,研究人员可以评估不同***干预措施对脑损伤的保护效果,寻找潜在的***靶点,并推动新药的研发。脑缺血...
-
 福建专门做脑缺血再灌注模型服务
发布时间:2024.02.25
福建专门做脑缺血再灌注模型服务
发布时间:2024.02.25
大鼠脑缺血再灌注造模在脑血管疾病研究中具有重要意义。通过模拟缺血再灌注的过程,研究人员可以评估不同***策略对脑损伤的影响,如给予药物、应用物理疗法或其他干预措施。这有助于寻找新的***方法和预防策略...
-
 广西真实的生物外包公司电话多少
发布时间:2024.02.24
广西真实的生物外包公司电话多少
发布时间:2024.02.24
生物外包公司是一种以生物技术为基础,以项目合作为形式,以创新为目标,以服务为理念的机构,它可以为各种生物领域提供专业的实验服务和技术支持。动物实验是生物外包公司的服务领域之一,它涉及到以下几个方面:(...
-
 山东有什么生物外包公司
发布时间:2024.02.24
山东有什么生物外包公司
发布时间:2024.02.24
生物外包公司是一种以客户需求为导向,以项目合作为基础,以创新为动力,以质量为保证,以服务为宗旨的机构,它可以为各个生物领域提供专业化、个性化、系统化的实验服务和技术支持。生物外包公司主要服务于生物医药...
-
 内蒙专业的生物外包公司有哪家
发布时间:2024.02.24
内蒙专业的生物外包公司有哪家
发布时间:2024.02.24
生物外包公司生物实验是一种多学科交叉的研究方法,它涉及到数学、物理、化学、计算机等多个领域的知识和技能。为了进行高水平的生物实验,我们需要掌握以下几方面的能力:(1)数学能力:能够运用数学公式、统计方...
-
 安徽专业的生物外包公司有哪家
发布时间:2024.02.23
安徽专业的生物外包公司有哪家
发布时间:2024.02.23
生物外包公司是一种利用生物技术为客户提供各种实验服务和技术支持的机构,它可以帮助客户节省实验时间和成本,提高实验质量和效率,解决实验难题和瓶颈。动物实验是生物外包公司的主要服务项目之一,它包括以下几个...
-
 云南靠谱的生物外包公司名字
发布时间:2024.02.23
云南靠谱的生物外包公司名字
发布时间:2024.02.23
生物外包公司生物实验是一种合作性的研究方法,它需要与不同的人或机构进行沟通和协作,以共享资源和信息,解决问题,达成共识和目标。为了进行有效的生物实验,我们需要具备以下几方面的能力:(1)沟通能力:...
-
 河南推荐的脑缺血再灌注模型多少钱
发布时间:2024.02.23
河南推荐的脑缺血再灌注模型多少钱
发布时间:2024.02.23
需要根据实验目的确定缺血时间和再灌注时间。缺血时间一般在30-120min之间,再灌注时间一般在24-72h之间。缺血时间越长,再灌注时间越短,损伤程度越重;反之,则损伤程度越轻。缺血时间和再灌注时间...
-
 南京市专业的生物外包公司有哪些
发布时间:2024.02.22
南京市专业的生物外包公司有哪些
发布时间:2024.02.22
生物外包公司是生物技术领域的重要参与者,它们在各种生命科学领域为客户提供的服务和解决方案。 生物外包公司是专门从事生命科学领域的公司,为制药、生物技术和研究机构提供一系列服务,包括生物样本分...
-
 甘肃推荐的生物外包公司有哪家
发布时间:2024.02.22
甘肃推荐的生物外包公司有哪家
发布时间:2024.02.22
生物外包公司可做分子检测实验还包括了分子诊断,生物外包公司可以为医疗机构提供快速、准确的分子诊断服务,帮助患者得到及时的诊断结果。一些生物外包公司专注于流式细胞仪和质谱仪等仪器的使用,用于基于分子检测...
-
 江苏推荐的生物外包公司电话多少
发布时间:2024.02.22
江苏推荐的生物外包公司电话多少
发布时间:2024.02.22
生物外包公司生物实验是一种合作性的研究方法,它需要与不同的人或机构进行沟通和协作,以共享资源和信息,解决问题,达成共识和目标。为了进行有效的生物实验,我们需要具备以下几方面的能力:(1)沟通能力:...
-
 贵州哪里有生物外包公司名字
发布时间:2024.02.21
贵州哪里有生物外包公司名字
发布时间:2024.02.21
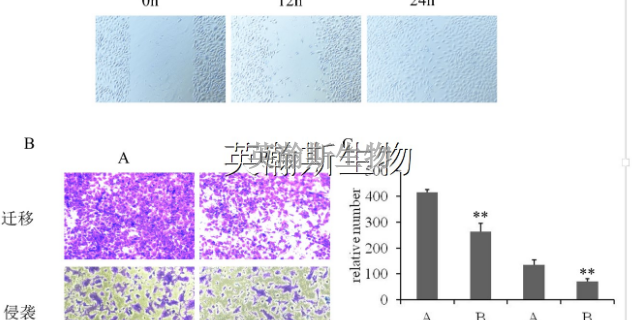
生物外包公司在免疫疫苗研究中,细胞实验可用于评估疫苗对免疫系统的效果。细胞实验在疾病研究中起着关键作用,例如研究、心血管疾病和传染病的研究。细胞实验也可用于研究细胞的运动和迁移,这对于了解胚胎发育和白...
-
 广西推荐的生物外包公司名字
发布时间:2024.02.21
广西推荐的生物外包公司名字
发布时间:2024.02.21
生物实验外包公司尽量要选择有整体性外包服务的公司。这样的公司一般在签订合同之前会给出一个整体评估方案,这样就能够在一定程度上判断一个公司是否靠谱。如果是不给实验前评估方案的公司极有可能再转手拆开外包出...
-
 云南专业的脑缺血再灌注模型多少钱
发布时间:2024.02.21
云南专业的脑缺血再灌注模型多少钱
发布时间:2024.02.21
大鼠脑缺血再灌注造模的建立涉及一系列的手术步骤。通常,研究人员会通过颈动脉结扎或大脑动脉结扎等方式暂时中断大鼠脑部的血液供应,然后再解除结扎,使血流再次灌注到脑组织中。这样的操作能够模拟脑缺血再灌注的...
-
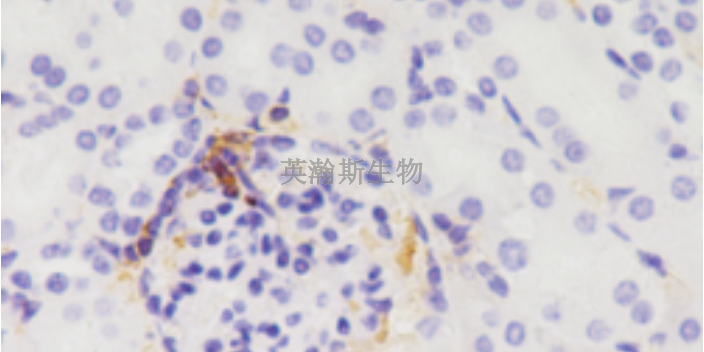
 海南专业的病理实验外包公司
发布时间:2024.02.21
海南专业的病理实验外包公司
发布时间:2024.02.21
病理实验外包,病理染色常见染色介绍免疫荧光染色:免疫荧光技术(Immunofluorescence technique )又称荧光抗体技术,是标记免疫技术中发展比较早的一种。它是在免疫学、生物化学和显...
-
 四川组织病理实验外包服务
发布时间:2024.02.21
四川组织病理实验外包服务
发布时间:2024.02.21
病理实验外包比较常见的实验是免疫组化染色,免疫组织化学的突出优点。1.高度的特异性:抗原--抗体反应是特异性比较强的反应之一。免疫组织化学所用的抗体必须是特异性强的多价或单价抗体,具有高度的识别能力,...
-
 江苏大鼠脑缺血再灌注模型检测
发布时间:2024.02.20
江苏大鼠脑缺血再灌注模型检测
发布时间:2024.02.20
需要注意的是,脑缺血再灌注模型具有一定的局限性。动物模型无法完全复制人类脑缺血再灌注损伤的复杂性和多样性。因此,研究人员在使用该模型时需要谨慎解释结果,并结合其他实验和临床数据进行综合分析。随着科学技...