商机详情 -
芜湖外泌体提取试剂
研究中研究人员发现,胃病细胞周围富含TAM。TAM以M2极化表型为特征,并促进胃病细胞在体外和体内的迁移。此外,研究人员发现M2衍生的外泌体决定了TAMs介导的迁移活动。通过使用质谱方法,研究人员确定载脂蛋白E(ApoE)是M2巨噬细胞衍生的外泌体中高度特异性和有效的蛋白质。ApoE是一种M2特异性且高度丰富的来源于M2外泌体的蛋白质,是决定胃病细胞迁移潜力的主要驱动因素。然而,来自ApoE-/-的小鼠M2巨噬细胞的外泌体在体外和体内对胃病细胞的迁移没有显着影响。在机制上,M2巨噬细胞衍生的外泌体介导ApoE启动的PI3K-Akt信号通路,并在TAM和受体胃病细胞之间进行细胞间转移,促进细胞骨架的迁移。总的来说,该研究发现外泌体介导的功能性ApoE蛋白从TAM转移到一些病症细胞,促进了胃病细胞的迁移。外泌体提取:磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点。芜湖外泌体提取试剂

来源于不同的组织的外泌体不仅具有其特异性蛋白分子,而且还包含其行使功能的关键分子。有关外泌体分泌和摄取及其组成、“运载物”和相应功能的精确分子机制近些年刚刚开始受到关注,与外泌体相关的被pubmed收录的文章数量和国自然基金项目中标数量逐年增长,表明国内外对外泌体的研究兴趣日益增长。细胞外囊泡是蛋白质、mRNA、miRNA和脂质运输来完成细胞间通讯通路的重要媒介,根据它们的大小和发生分为三类,包括外泌体、微泡和凋亡小体。其中,外泌体是直径大约为40-100nm的包装囊泡,由多种细胞分泌,内含有特定的蛋白质、脂质、细胞因子或遗传物质。深圳正规外泌体提取试剂产品介绍用于外泌体提取的体液收集注意事项:注意抗凝剂的选择。
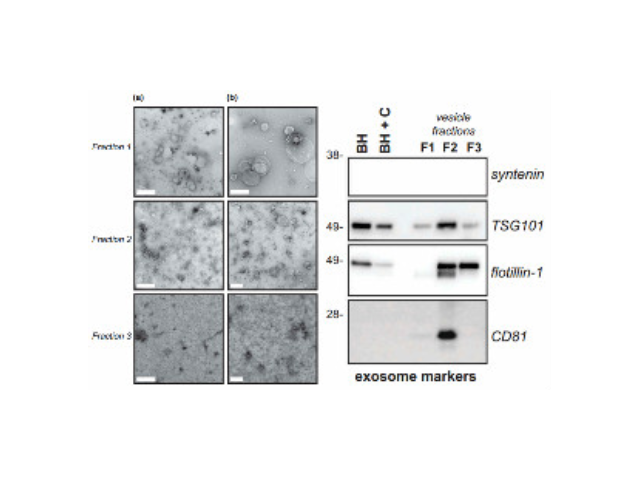
外泌体的形成与鉴定:首先,细胞膜内陷形成一个杯状结构,包括细胞表面蛋白和与细胞外环境相关的可溶性蛋白,导致早期胞内体(early-sortingendosome,ESE)的从头形成,或者是杯状结构直接和已经存在的ESEs融合;trans-高尔基体和内质网也能协助形成ESEs。ESE成熟后形成晚期胞内体(late-sortingendosomes,LSEs),较终形成MVBs(也称为多囊内小体)。MVBs是通过endosome限制膜向内凹(即质膜双凹)形成的,这一过程导致MVBs含有多个ILVs。MVB可以与溶酶体或自噬体融合,较终降解或与质膜融合释放作为外泌体的ILVs。外泌体表面蛋白包括四聚体蛋白、整合蛋白、免疫调节蛋白等。外泌体可以包含不同类型的细胞表面蛋白、细胞内蛋白、RNA、DNA、氨基酸和代谢物。使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后。
外泌体是指包含了复杂RNA和蛋白质的小膜泡(30-150nm),现今,其特指直径在40-100nm的盘状囊泡。1983年,外泌体初次于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“exosome”。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。所有培养的细胞类型均可分泌外泌体,且外泌体天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中。有关他们分泌和摄取及其组成、“运载物”和相应功能的精确分子机制刚刚开始研究。外泌体目前被视为特异性分泌的膜泡,参与细胞间通讯,对外泌体的研究兴趣日益增长,无论是研究其功能还是了解如何将其用于微创诊断的开发。外泌体提取:免疫分离外泌体的原理大多是通过抗体包被的微球,特异性结合外泌体。
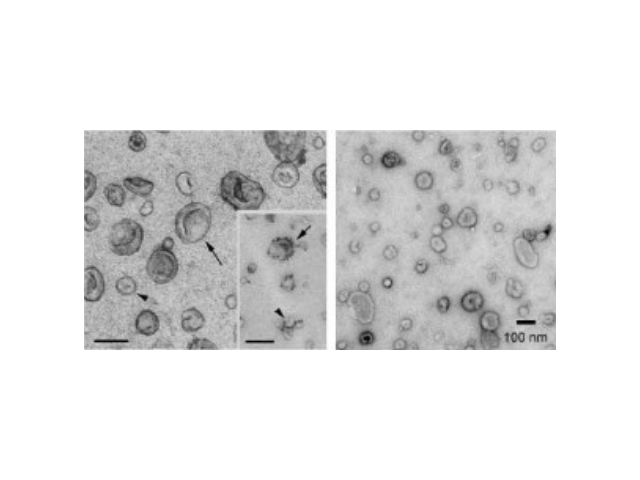
外泌体与肺病预后:外泌体mirRNA和蛋白质被认为是NSCLC的预后因子。Dejima等在研究NSCLC患者预后的生物标志物时发现,外泌体miR-4257和miR-21的含量显着上升。此外,还有研究表明,低水平miR-146a-5p的NSCLC患者较高水平miR-146a-5p的NSCLC患者有更高的复发率。Sandfeld-Paulsen等在研究276例NSCLC患者血浆的外泌体时发现,NY-ESO-1是其中对低生存率有显着影响的标志物。Silva等利用TaqMan低密度芯片的方法系统分析了28位NSCLC患者体内的365种miRNA,其中let-7f、miR-30e-3p和miR-20b表达均下调,进一步研究发现,let-7f和miR-30e-3p水平可以区分早期和晚期NSCLC患者,高水平let-7f和miR-30e-3p与不良预后密切相关。超滤离心法简单高效,且不影响外泌体的生物活性,是提取细胞外泌体的一种新方法。天津正规外泌体提取试剂厂家直销
外泌体提取:可以将不同的洗脱溶液应用于该方法。芜湖外泌体提取试剂
为了分离外泌体,研究人员用两个这样的单元串联构建了一个装置。首先,使用声波从血液样品中除去细胞和血小板。一旦细胞和血小板被去除,样品进入第二个微流体单元,然后使用较高频率的声波将外泌体与稍大的细胞外囊泡分开。这项工作的通讯作者之一,麻省理工学院材料科学与工程系科学家MingDao博士说:“声波更温和。而且在分离时,这些囊泡受处理的时间只有1秒钟或更短。这是一个很大的优势。”使用该设备,处理100微升未稀释血液样本只需要不到25分钟。“这种新技术可以解决当前外泌体分离技术的缺点,如周期长,一致性差,产量低,污染以及完整性受损等。我们想要把提取高质量的外泌体的过程简化为按一个按钮就在10分钟内获得所需样品一样简单。”研究人员们说。芜湖外泌体提取试剂