商机详情 -
进口激光荧光双光子显微镜成像原理
像差问题一直困扰着光学领域的工作者。像差会使光波前发生形变,不仅降低成像的信噪比和分辨率,使得很多时候我们只能“雾里看花”,更甚者,产生赝像,或无法获得有意义的图像。像差问题对双光子成像的影响尤为严重,因为在那里,荧光信号对入射光强度的依赖是平方关系,一旦入射光波前形变,不仅聚焦强度大幅下降,成像分辨率也急剧恶化。因此,如何解决像差问题,实现,例如小鼠大脑皮层,深层区域的高质量成像成为光学成像发展中相当有挑战性的问题之一。双光子显微镜使用方法是什么?进口激光荧光双光子显微镜成像原理

新一代微型化双光子荧光显微成像系统的成功研制是国家重大科研仪器研制专项的一个硕果。它彰显了北京大学在生物医学成像领域先期布局的前瞻性,锻炼了一支以年轻PI和硕博研究生为主体、具有学科交叉背景和重要技术创新能力的“中国智造”队伍。目前,该研发团队正在领衔建设“多模态跨尺度生物医学成像”十三五国家重大科技基础设施,积极参与即将启动的中国脑科学计划。可以期待,微型化双光子荧光显微成像系统将为实现“分析脑、理解脑、模仿脑”的战略目标发挥不可或缺的重要作用激光荧光双光子显微镜荧光寿命计数双光子显微镜观察到的现象证明了钙离子的增加依赖于肌体触发的钠离子作用电势。

为了验证动物生物样品的时间分辨成像能力,本实验观察了活海拉细胞高尔基体中的青色荧光蛋白mTFP1,见图3(a),(c)-(i)。使用的物镜及尺寸与荧光颗粒成像一致,对比可见v2PE在空间分辨率、激发深度级图像对比度较常规宽场显微镜都有所提高。此外,v2PE可以同时激发多个波长的荧光蛋白,这种技术还可以应用于细胞内分子的三维动力学多色成像。在此基础上,实验对海拉细胞中的高尔基体(mTFP1)和纤颤蛋白(EGFP)进行了在体成像,见图3(j)-(n),青色为mTFP1,绿色为EGFP,实验中两种荧光蛋白同时成像,终采用光谱分离法将不同蛋白的荧光信号分离出来。
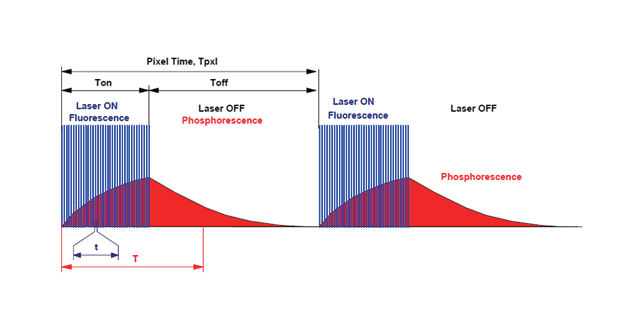
双光子显微镜的基本原理是:在高光子密度的情况下,荧光分子可以同时吸收 2 个长波长的光子,在经过一个很短的所谓激发态寿命的时间后,发射出一个波长较短的光子;其效果和使用一个波长为长波长一半的光子去激发荧光分子是相同的。双光子激发需要很高的光子密度,为了不损伤细胞,双光子显微镜使用高能量锁模脉冲激光器。这种激光器发出的激光具有很高的峰值能量和很低的平均能量,其脉冲宽度只有 100 飞秒,而其周期可以达到 80至100兆赫兹。在使用高数值孔径的物镜将脉冲激光的光子聚焦时,物镜的焦点处的光子密度是比较高的,双光子激发只发生在物镜的焦点上,所以双光子显微镜不需要共聚焦,提高了荧光检测效率。双光子显微镜只有焦平面处才能形成双光子吸收,而焦平面之外由于光强低无法被发动,所以双光子成像更清晰。
2020年12月22日,临研所、病理科和科研处邀请北京大学王爱民副教授做了题目为“新一代微型双光子显微成像系统介绍及其在临床医疗诊断”的学术报告。学术报告由临研所医学实验研究平台潘琳老师主持。王爱民,北京大学信息科学技术学院副教授,毕业于北京大学物理系,获学士、硕士学位,后于英国巴斯大学物理系获博士学位。该研究组研发的微型双光子显微镜,第1次在国际上获得了小鼠大脑神经元和神经突触清晰稳定的动态信号,该成果获得了2017年度“中国光学进展”和“中国科学进展”,并被NatureMethods评为2018年度“年度方法--无限制行为动物成像”。目前,该研究组正在研究新一代双光子显微成像技术在临床诊断中的应用,为未来即时病理、离体组织检测、术中诊断等提供新的影像手段和分析方法。双光子显微镜在组织透明化成像中应用。国内investigator双光子显微镜分辨率是多少
双光子显微镜为什么穿透能力强?进口激光荧光双光子显微镜成像原理
研究人员通过用不同激光波长并行化激光扫描(wavelengthmultiplexing),增加了相同时间内可以成像的体积,并同时保持较高的时间和空间分辨率。通过引入两种波长不同的钙信号荧光探针,研究人员将神经元群体的活动标记为两个不同颜色,并同时用两个不同波长的激光激发探针,实现了两个颜色的并行化数据记录。为了实现三维空间成像,研究人员还分别在两个激光光路上配置了快速变焦系统,分别为电可调节透镜(electricaltunablelens)和空间光调制器(spatiallightmodulator)。由此,可以同时以10赫兹的速度记录500微米500微米的10个平面,覆盖纵深达600微米,涵盖了从脑皮层第2层到第5层的结构,体积内记录到的神经元可以达到2000个以上。进口激光荧光双光子显微镜成像原理