商机详情 -
外泌体提取试剂哪里买
研究加深了对疟原虫传染宿主所分泌的外泌体与一些病症血管生成之间的相互作用的认识,为开发疟原虫传染来源的外泌体作为一种新型抗一些病症制剂奠定了基础。研究人员选用肺病小鼠模型作为研究对象,从传染疟原虫的小鼠血浆中获得外泌体,并将这些外泌体注射到小鼠的一些病症内部,并与没有疟原虫传染的小鼠血浆外泌体进行对照。研究发现,疟原虫传染小鼠的血浆外泌体明显压制一些病症血管的生成。进一步的研究发现,疟原虫传染的小鼠血浆外泌体通过至少四种特殊的微小RNA(miR16-5p/17-5p/322-5p/497-5p)压制血管内皮细胞VEGF受体(VEGFR2)的表达从而阻断血管生成的信号通路。这些发现加深了人们对疟原虫抗病机理的理解,并为疟原虫疗法治病一些疾病的临床研究提供进一步的理论依据。研究初次发现疟原虫传染小鼠血浆外泌体(exosomes)能够压制一些病症血管生成,并初步阐明其分子机制。外泌体提取:密度梯度离心。外泌体提取试剂哪里买
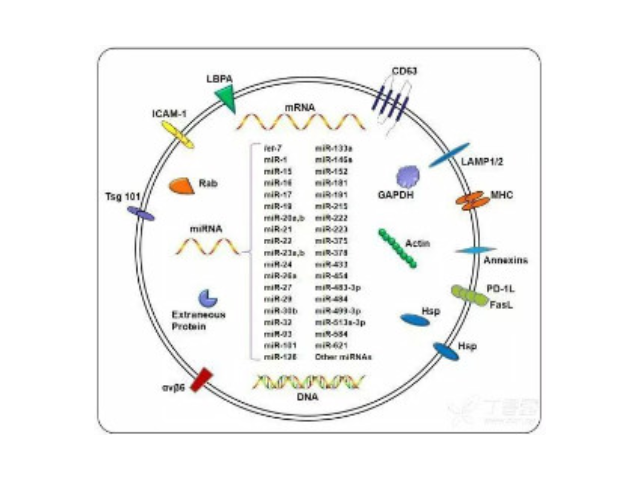
外泌体(exosomes,Exos)是细胞分泌的一种膜囊泡,因其可以将供体细胞的信息通过其携带的蛋白质、mRNA、miRNA等传递到受体细胞,实现细胞之间的信息交流及物质交换,并且可以作为药物载体转运药物而引起科学家的普遍关注(Fig1)。外泌体作为内源性的天然药物载体有着独特的优势,表面由脂质和蛋白质组成,使其可以穿透许多生物膜,提高药物的运输效率和靶向性,可以稳定存在于血液中,纳米级尺寸明显增强药物在瘤部位的渗透滞留效应(permeabilityandretentioneffect,EPR)。目前,许多抗药物、基因药物及药物均被成功载入外泌体。但是由于没有较好的外泌体分离纯化和载药的方法,使得其作为药物载体的应用受到限制。上海外泌体提取试剂哪家便宜外泌体提取:低速离心去除细胞和凋亡碎片。

人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA。
外泌体研究的主要应用:外泌体的功能取决于其所来源的细胞类型,其可参与到机体免疫应答、抗原提呈、细胞迁移、细胞分化、一些病症侵袭等方方面面。有研究表明一些病症来源的外泌体参与到一些病症细胞与基底细胞的遗传信息的交换,从而导致大量新生血管的生成,促进了一些病症的生长与侵袭。一些病症。一些病症转移。来自白血病干细胞的外泌体促进急性骨髓性白血病(AML)细胞的增殖、迁移和压制细胞凋亡。治病靶标。利用外泌体递送小干扰RNA来沉默KRASG12D,从而特异性高效靶向至胰腺病细胞,以明显降低RAS活化、病细胞增殖和转移过程。免疫。β细胞将含有蛋白质和miRNA的外泌体释放到细胞外,并可转移到其他代谢部位或免疫内皮细胞,有利于维持葡萄糖体内平衡或造成胰岛素抵抗。心血管。外泌体介导miR-155从平滑肌细胞转移到内皮细胞导致了内皮细胞的损伤促进动脉硬化。分子标记。疾病诊断。在酒精性肝病、NASH、菌类性肝炎、药物性肝损伤和肝细胞病中发现循环EVs的水平上升。预后标志。外泌体(Exosome)发现于1986年,是一种直径约30~100nm的双层膜囊泡状结构小体。

外泌体的提取分离:1、PEG-base沉淀法。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等,因此发表文章时易受质疑。2、试剂盒提取。近几年来,市场上已出现各种商业化的外泌体提取试剂盒,有的是通过特殊设计的过滤器过滤掉杂质成分,有的则采用空间排阻色谱法(SEC)进行分离纯化,也有的则利用化合物沉淀将法外泌体沉淀出来。这些试剂盒不需要特殊设备,随着产品不断更新换代,提取效率和纯化效果逐渐提高,因而逐渐取代超速离心法并推广开来。有些试剂盒操作简便,不用超速离心,同时可获得高纯度和高回收率的外泌体。超滤离心法简单高效,且不影响外泌体的生物活性,是提取细胞外泌体的一种新方法。外泌体提取试剂平均价格
外泌体作为内源性的天然药物载体有着独特的优势,表面由脂质和蛋白质组成。外泌体提取试剂哪里买
外泌体的提取主要包括以下几种方式:一是超速离心法,这是目前外泌体提取较常用的方法。此种方法得到的外泌体量多,但是纯度不足,电镜鉴定时发现外泌体聚集成块,由于微泡和外泌体没有非常统一的鉴定标准,也有一些研究认为此种方法得到的是微泡不是外泌体。二是过滤离心,这种操作简单、省时,不影响外泌体的生物活性,但同样存在纯度不足的问题。三是密度梯度离心法,用此种方法分离到的外泌体纯度高,但是前期准备工作繁杂,耗时,量少。四是免疫磁珠法,这种方法可以保证外泌体形态的完整,特异性高、操作简单、不需要昂贵的仪器设备,但是非中性pH和非生理性盐浓度会影响外泌体生物活性,不便进行下一步的实验。五是PS亲和法,该方法将PS(磷脂酰丝氨酸)与磁珠结合,利用亲和原理捕获外泌体囊泡外的PS。该方法与免疫磁珠法相似,获得的外泌体形态完整,纯度较高。由于不使用变性剂,不影响外泌体的生物活性,外泌体可用于细胞共培养和体内注射。2016.9《ScientificReports》杂志发表了该方法较新数据,表明PS法可提取相当高纯度的外泌体。六是色谱法,这种方法分离到的外泌体在电镜下大小均一,但是需要特殊的设备,应用不普遍。外泌体提取试剂哪里买